עיתונאיות ועיתונאים, הירשמו כאן להודעות לעיתונות שלנו
הירשמו לניוזלטר החודשי שלנו:
מדעני מכון ויצמן חשפו חלק מהמנגנונים המולקולריים האחראים למערכת הפרופריוספציה – חישה עצמית של תנוחת איברי גופנו ותנועתם

עִצמו את עיניכם ונסו לגעת באפכם באמצעות האצבע המורה. רובנו מסוגלים לבצע תנועה זו בדיוק רב, אבל איך אנחנו יודעים לאתר את האף שלנו במרחב ללא חוש הראייה? ואיך אנו מצליחים לעקוב אחר המיקום של הזרוע תוך כדי תנועתה? "מעטים יודעים שבנוסף לחמשת החושים שלנו – ראייה, שמיעה, ריח, מגע וטעם – קיים גם מה שמכונה לעיתים 'החוש השישי' – תחושת המיקום במרחב", אומר פרופ' יורם גרונר, מהמחלקה לגנטיקה מולקולרית במכון ויצמן למדע. מודעות גופנית שכזו, המכונה גם פרופריוספציה, מתייחסת לחישה עצמית של תנוחת איברי גופנו ושל תנועתם.
כאשר קיימות הפרעות נוירולוגיות, נפגעת לעיתים קרובות מערכת הפרופריוספציה, ולכן, מבחן פשוט של ״אצבע-אל-אף״ משמש רופאים לאבחון ראשוני של הפרעות אלו או לשלילתן. אולם, על אף שהפרופריוספציה היא אחת ממערכות ה"חיווט" העצבי הפשוטות בגוף, המנגנונים המולקולריים האחראים ליצירת תחושת התנוחה במרחב עדיין אינם מובנים דיים.
במחקר שנמשך לאורך מספר שנים במעבדתו של פרופ' גרונר גילו מדענית הסגל מן המניין ד"ר דיצה לבנון ועמיתיה, כי חלבון מסוים – גורם שיעתוק Runx3 – הוא בַּקָר חיוני להתפתחות ולתיפקוד של תאי עצב (נוירונים) מסוג TrkC, שהם נוירוני חישה מיוחדים בעלי חשיבות בפרופריוספציה. מסבירה ד"ר לבנון: "מצאנו כי אובדן פעילות Runx3 קשור לתמותת תאי TrkC בגנגליונים שבצידי עמוד השדרה בעכברים, וכתוצאה מכך הם מפתחים אטקסיה, כלומר מאבדים את היכולת למקם את רגליהם במקום הנכון ואת יכולתם לשלוט בתנועתן ובאיזון גופם. למרות שמקטע ה-DNA אשר מקודד את Runx3 נוכח בכל תאי הגוף, ומן הסתם גם בסוגים אחרים של עצבי חישה, הגן 'מופעל' – כלומר, משועתק ומתורגם לחלבון – רק בתאי חישה מסוג TrkC, והשאלה שאנחנו מנסים לענות עליה היא, מה בדיוק 'מפעיל' ו'מכבה' את הגן Runx3 במקום ובזמן הנכונים, ובכך מוביל להיווצרות תאי עצב מסוג זה".
מעטים יודעים שבנוסף לחמשת החושים שלנו – ראייה, שמיעה, ריח, מגע וטעם – קיים גם מה שמכונה לעיתים 'החוש השישי' – תחושת המיקום במרחב"
ד"ר לבנון ועמיתיה – ד"ר אלנה אפל, ד"ר קירה אורלובסקי וד"ר יהודה זלצברג – גילו שלושה שחקני מפתח אשר מנהלים את שיעתוק הגן Runx3, ובדרך זו מעורבים בהתפתחות ובתפקוד הפרופריוספציה. על מנת להתחיל ב"שיעתוק גן", הצעד הראשון בתהליך שבו הופך הגוף את המידע המקודד בגן לחלבון, נקשרים גורמי שעתוק לרצף מסוים ב-DNA בסביבות הגן אשר מתפקד כמקטע מאתחל (פרומוטור) של תהליך השיעתוק. אבל מערך הבקרה השולט על השיעתוק הוא מורכב, וכולל גורמי בקרה נוספים, ולכן עולה בעיה נוספת: כיצד לאתר והיכן לחפש את הבקרים הגנטיים המעורבים בשיעתוק הגן Runx3.
כדי להתמודד עם קושי זה השתמשו המדענים בכרומוזומים מלאכותיים של חיידקים (BACs), הנושאים בקרבם מקטעים גדולים של DNA עכברי, ויצרו עכברים מהונדסים גנטית שהכילו BACs נושאי הגן Runx3, ובכלל זה האזורים הגנומיים הסמוכים לו. בנוסף, כדי לאפשר מעקב אחר התבטאות של Runx3, הוכנס לתוך Runx3 שב-BACs גן מדווח פלואורסצנטי (GFP), אשר שימש כגלאי פעילות של הגן. "חקירת דפוס הביטוי של הגן המדווח בעכברים מהונדסים המכילים BACs, איפשרה לנו לגלות איזור מרוחק אשר אחראי על ביטוי ספציפי של Runx3 בתאי עצב מסוג TrkC, ומכיל את גורמי הבקרה שאותם חיפשנו", מסביר פרופ' גרונר. מוסיפה ד"ר לבנון: "היות שביטויו של הגן Runx3 בתאי עצב מסוג TrkC השתמר לאורך האבולוציה, סברנו כי גורמי הבקרה שלו השתמרו אף הם, ולכן השווינו את המקטע הכולל את גורמי הבקרה שזיהינו בניתוח התוצאות שהתקבלו מעכברי BACs מהונדסים, לאזורים מקבילים בגנומים של בני אדם, עופות, צפרדעים ודגים. ההשוואה איפשרה לנו לזהות שלושה מקטעים גנומיים באיזור מרוחק מהגן Runx3, שהיו משותפים לכולם". שלושת בקרי השיעתוק הללו כונו: R2, R1 ו-R3.
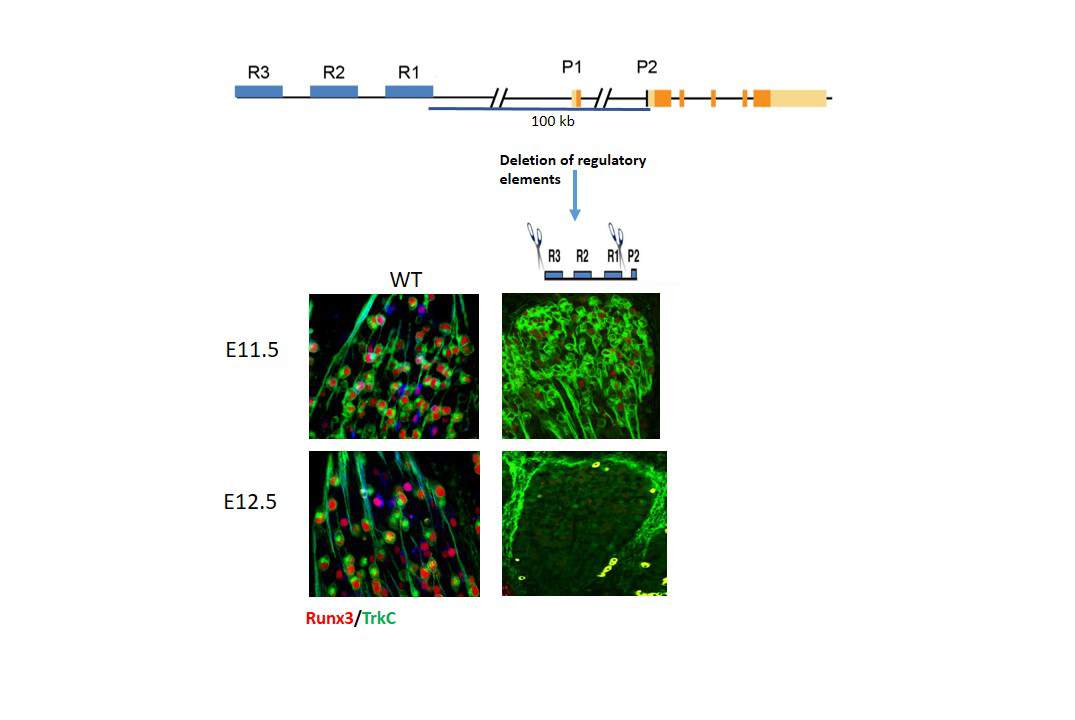
כדי להוכיח באופן חד-משמעי כי בקרי שעתוק (R) אלו אכן מבקרים את ביטויו של Runx3, השתמשו המדענים בשיטת מחקר חדשנית הנעזרת ב-CRISPR/Cas9 כדי להשמיט מגנום העכברים את כל אחד מאזורי הבקרה, בנפרד או בזוגות. הממצאים, שפורסמו באחרונה בכתב העת Genes & Development, מראים בבירור כי למחיקת שניים מתוך שלושת גורמי הבקרה – R1 ו-R3 – הייתה השפעה זהה לזו של השמטת כל הגן Runx3 עצמו; כלומר, עכברים שבהם לא היו שני המקטעים הגנטיים הקצרים הללו, פיתחו אטקסיה.
המשך המחקר העלה, כי לצורך ההתפתחות הספציפית של תאי עצב מסוג TrkC אין די בכך שהבקרים מנהלים את שיעתוקו של Runx3 ומזרזים התבטאותו בתאי עצב מסוג TrkC; במקביל הם גם פועלים לדכא את ביטויו בתאי עצב מסוגים אחרים. יתר על כן, החוקרים גם עמדו על תפקידו הייחודי של כל בקר, דבר שהוביל לגילוי ולאיפיון של תת-אוכלוסיות של תאי TrkC: בשלבים מוקדמים של ההתפתחות העובר העכברי, באמצע היום ה-12, פועלים שלושת הבקרים – R2, R1 ו-R3 – יחדיו בניהול ביטויו של Runx3 בתאי עצב מסוג TrkC, אבל עם ההתפתחות העוברית, מתחיל לפעול מנגנון מורכב של השפעות גומלין בין שלושת הבקרים. מנגנון זה מנהל את ביטוי הגן בתאי עצב מסוג TrkC ובתת-סוגים של תאי המערכת הפרופריוספטורית.
"חשיבותן של תוצאות אלו נובעת מכך, שקיים רק קומץ מחקרים המתעדים את התקשורת בין בקרי שיעתוק לבין הגנים שהם מנהלים בגוף החי עצמו, ולא במבחנה״, אומרת ד"ר לבנון. "בעתיד, ייתכן שניתן יהיה להשתמש בשלושת בקרי השיעתוק שגילינו על מנת להתמקד בתאי עצב TrkC במקרים של אטקסיה ובמחלות עצביות אחרות שבהן מעורב Runx3".