עיתונאיות ועיתונאים, הירשמו כאן להודעות לעיתונות שלנו
הירשמו לניוזלטר החודשי שלנו:
שתי תעלומות ביולוגיות, שפער של מיליארדי שנים מפריד ביניהן, נפגשו במחקר שנערך באחרונה במכון ויצמן למדע.
התעלומה הראשונה היא הגדולה מכולן – מקור החיים. ליתר דיוק, מקור החלבונים – אותן מולקולות ביולוגיות החיוניות לקיומם של חיים כפי שאנו מכירים אותם. כיצד נוצרו מכונות מולקולריות מורכבות ומשוכללות אלה ממקטעי חלבון קצרצרים שצפו להם ב"מרק הקדום" – הסביבה המימית הקדמונית והעשירה במינרלים ששררה, לפי ההשערות, בכדור-הארץ לפני כארבעה מיליארד שנים?

כדי להשיב על שאלה זו, בנו מדענים במעבדתו של פרופ' דן תופיק המנוח במחלקה למדעים ביומולקולריים של המכון, יחד עם שותפיהם למחקר, מודל מתמטי שמטרתו לשחזר את האב הקדמון האבוד של החלבונים המודרניים. על-פי המודל שיצרו, האב הקדמון היה מורכב משני מקטעי חלבון קצרצרים הקרויים פפטידים, שהיו בעלי רצף כמעט זהה של חומצות אמינו – אבני הבניין של החלבונים. במלים אחרות, החלבון הקדום הורכב מ"מלה" מולקולרית שחזרה על עצמה פעמיים ויצרה מעין "משפט" מולקולרי קדמוני.
כדי לשחזר את תהליך היווצרותו של החלבון במעבדה, יצרו המדענים את האב הקדמון המשוער שלהם ואז חתכו אותו לשניים – פפטיד ועוד פפטיד – והכניסו אותם לסביבה מימית, במטרה לראות מה יתחולל והאם ה"מלים" יתחברו ל"משפט". בשלב הראשון לא נצפו סימנים לחיבורים, אך כאשר ד"ר ליאם לונגו, אז חוקר בתר-דוקטוריאלי במעבדתו של פרופ' תופיק, הוסיף לתמיסה אר-אן-אי – מולקולות שהיו לפי ההשערות נפוצות במרק הקדום – המים נעכרו באחת. בעזרת מיקרוסקופ גילה ד"ר לונגו כי הפפטידים, בעלי המטען החיובי, נקשרו למולקולות האר-אן-אי, בעלות המטען השלילי, ובנוזל המימי נוצרו טיפות בתהליך של הפרדת פאזות – בדומה לטיפות שומן במרק עוף.

"זו הייתה תגלית מרגשת כי קיומן של טיפות כאלה במרק הקדום יכול היה להגדיל את הסיכוי לחיבורים בין פפטידים וליצירתו של האב הקדמון של החלבונים, כפי שנחזה במודל", נזכר ד"ר לונגו, העומד כיום בראש קבוצת מחקר משלו במכון לטכנולוגיה של טוקיו.
קפיצה קטנה בזמן – מהעידן שקדם להופעת החיים בכדור-הארץ היישר לתחילת המאה ה-21. לפני כעשור, התגלה כי טיפות דומות לאלו שלכאורה נוצרו במרק הקדום, נוצרות באופן טבעי בתאי גופנו ואף הן מורכבות מחלבונים או משילוב של חלבונים ומולקולות אר-אן-אי או די-אן-אי. בשנת 2018 כיכבו הטיפות ברשימת המועמדות לתואר "פריצת הדרך המדעית של השנה" של כתב-העת המדעי Science והן הוכתרו "אחד הנושאים החמים בביולוגיה של התא". ואכן, בכל הקשור לטיפות, רב עדיין הנסתר על הגלוי: כך למשל, לא ידוע עדיין אם הן משמשות לאחסון בלבד או שיש להן תפקידי בקרה בתא.
בנקודה זו בדיוק הצטלבו דרכיהן של שתי התעלומות הביולוגיות: פרופ' תופיק יצא לחקור את תפקידן הפוטנציאלי של הטיפות בהיווצרות חלבונים קדומים, ובשלב זה היה ברור שהממצאים צפויים לשפוך אור חדש גם על השפעתן של הטיפות כיום על בריאות האדם.
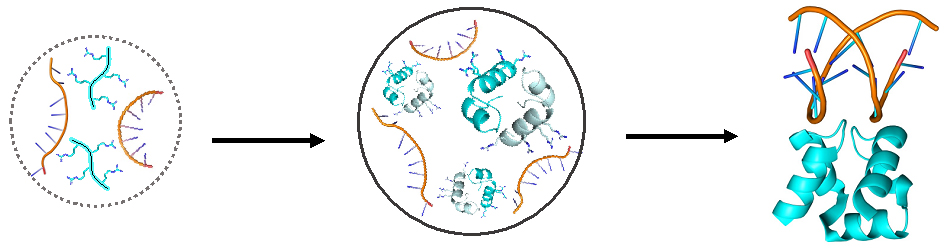
פרופ' תופיק ועמיתיו שיערו כי הטיפות שנוצרו במרק הקדום בעקבות מפגשים בין פפטידים למולקולות אר-אן-אי שימשו מעין תאים ראשוניים, פרוטו-תאים, שאולי בהמשך הדרך התפתחו לתאים החיים שאנו מכירים כיום .לפי ההשערה, הטיפות יצרו חללים סגורים ונפרדים שאפשרו לקרב ולחבר בין פפטידים שאחרת אולי לא היו מוצאים זה את זה במרחבי המרק הקדום. קרבה זו יכלה לאפשר לפפטידים להתארגן למבנים כימיים פשוטים הקרויים דימרים: זוגות פפטידים הנמשכים זה לזה באמצעות כוחות מולקולריים. בשלב הבא הדימר התאחה לכדי מולקולה אחת, וכך נוצר אותו אב קדמון שחזו המדענים.
כדי לאשש השערה זו, היה על המדענים למצוא תחילה ראיות לקיומם של דימרים באותה תמיסת פפטידים שיצרו, אך השיטות הסטנדרטיות לא אפשרו להם להגיע לרזולוציה גבוהה מספיק. כדי להתגבר על בעיה זו, פרופ' תופיק וקבוצתו שיתפו פעולה עם פרופ' דניאלה גולדפרב מהמחלקה לפיסיקה כימית וביולוגית של המכון, החוקרת חלבונים באמצעות תהודה אלקטרונית פאראמגנטית.
""זה שובר את לבי שדני לא זכה לראות את הממצא הזה", אומר ד"ר לונגו. "הוא כל-כך רצה לראות את הדימרים האלה"
"שיתוף הפעולה הזה נבע מהחברות שלי עם דני", נזכרת פרופ' גולדפרב בפנייתו של פרופ' תופיק. "הוא סיפר לי שיש לו תיאוריה לגבי האבולוציה של חלבונים, והצעתי לבחון אותה בעזרת היכולות של המעבדה שלי". פרופ' גולדפרב וקבוצתה החלו לחפש את הדימרים המשוערים של פרופ' תופיק בשיטות חדשניות: הם סימנו פפטידים באמצעות תגיות ספין אלקטרוני – מולקולות קטנטנות בעלות תכונות מגנטיות ייחודיות אשר הוכנו במעבדתו של פרופ' נורמן מטאנס באוניברסיטה העברית בירושלים. כאשר הוכנסו הפפטידים המתויגים לשדה מגנטי, התגיות נהפכו ל"מרגלות" המעבירות מידע על תכונות הפפטידים שאליהם הן מחוברות. כך, באמצעות שיטת דימות המכונה "תהודת אלקטרונים כפולה" (double electron-electron resonance, או DEER), יכלו המדענים לקבוע את המרחק בין פפטיד אחד למשנהו על-פי עוצמת האינטראקציות המגנטיות בין התגיות; קִרבה גדולה בין שני פפטידים הצביעה למעשה על היווצרותו של דימר.
מערך ניסויי זה היה מאתגר במיוחד, ובמדידות הראשונות לא הצליחו החוקרים לאתר דימרים כלל. בעיצומם של החיפושים קרה אסון. ב-4 במאי 2021 נפל פרופ' תופיק אל מותו בתאונת טיפוס הרים. רצה הגורל, ודווקא למחרת מצא ד"ר מנאס סיל, חוקר בתר-דוקטוריאלי במעבדתה של פרופ' גולדפרב, את הדימרים הראשונים בתמיסה של פפטידים. "זה שובר את לבי שדני לא זכה לראות את הממצא הזה", אומר ד"ר לונגו. "הוא כל-כך רצה לראות את הדימרים האלה".

השלב הבא היה להראות כי הדימרים נוצרים לא רק בתמיסה של פפטידים, אלא גם בתוך הטיפות עצמן – כאשר הפפטידים מחוברים למולקולות אר-אן-אי. תחילה הראו המדענים כי הפפטידים אכן נקשרים לאר-אן-אי בתוך הטיפות, באמצעות תצפיות שהציגו האטה בתנועתן של התגיות המרגלות. ואולם את השלב הבא – יצירת הדימרים – היה קשה להראות בשל הדוחק הרב בתוך הטיפות. בסופו של דבר, לאחר בדיקה של ריכוזים שונים של אר-אן-אי ופפטידים בטיפות, הצליחו המדענים להוכיח כי גם בתוכן נוצרים דימרים.
"בעצם הראינו שהקישור למולקולות האר-אן-אי מגביר את היווצרות הדימרים", אומר ד"ר סיל, שהוביל את הניסויים. "הקישור הזה כנראה עוזר לפפטידים למצוא זה את זה, כמו שני אנשים האוחזים בקצוות של אותו חבל".
ממצאים אלה מחזקים מאוד את השערתו של פרופ' תופיק, שלפיה הטיפות שנוצרו במרק הקדום קידמו שלב מכריע באבולוציה של החלבונים – יצירת דימרים מזוגות פפטידים כחוליה בדרך ליצירת חלבונים ארוכים יותר – ולפיכך תרמו להופעת החיים בכדור-הארץ. "'ערש האבולוציה של החלבונים', כך קראנו לטיפות במאמר שלנו", מציין ד"ר לונגו.

מלבד הבנה טובה יותר של ראשית החיים, תובנות חדשות אלה עשויות לתרום בעתיד גם להבנה של בריאות האדם. כך למשל, לפי סברות שונות, פגמים בהיווצרות הטיפות בתאים שלנו עלולים להביא להתפתחותן של מחלות מוח ניווניות. לפיכך, היכרות מעמיקה יותר עם מנגנוני היווצרות הטיפות ותפקידיהן עשויה לסלול את הדרך לשיטות אבחון וטיפולים חדשים.
במחקר השתתפו גם ד"ר דרגאנה דספוטוביץ' ממעבדתו של פרופ' תופיק המנוח; אורית ווייל-קטורזה ופרופ' נורמן מטאנס מהאוניברסיטה העברית בירושלים; ופרופ' יעקב לוי מהמחלקה לביולוגיה כימית ומבנית של המכון.
בתאים שלנו, חלבונים הנמצאים בתוך טיפות יכולים להגיע לריכוז של 3 עד 15 מיקרומולר – פי כמה מאות יותר מאשר ריכוזם בנוזל התא.