לקבלת מידע נוסף, תמונות ולתיאום ראיונות:
משרד הדוברת - מכון ויצמן למדע
08-9343856 news@weizmann.ac.il
עיתונאיות ועיתונאים, הירשמו כאן להודעות לעיתונות שלנו
הירשמו לניוזלטר החודשי שלנו:
עד לפני כמה שבועות היה נראה כי החיסונים מסמנים לעולם את הדרך החוצה מהמגיפה, אך הופעתם המתמדת של וריאנטים חדשים מחדדת את ההבנה כי לצד חיסונים יש צורך דחוף גם בטיפול תרופתי יעיל נגד נגיף הקורונה. במחקר המתפרסם בכתב-העת המדעי Nature Microbiology פיתחו מדעני מכון ויצמן למדע – בשיתוף פעולה עם מכון פסטר בצרפת והמכונים הלאומיים לבריאות (NIH) בארצות-הברית – גישה טיפולית חדשה: במקום להתמקד ב"חלבון הכתר" של הקורונה האחראי לכניסת הנגיף לתאי הגוף, הפנו החוקרים את הזרקור פנימה – אל החלבון הממוקם על קרומי התאים שלנו ומהווה את שער הכניסה של הנגיף. באמצעות שיטות מתקדמות של "אבולוציה במבחנה", פיתחו החוקרים מולקולת חלבון קטנה הפועלת כ"פקק" אשר חוסם את כניסת הנגיף לתאי הגוף, ועשויה להפוך לתרופה לקורונה.
חלק ניכר מטיפולי הקורונה שמצויים כיום בפיתוח – ומהחיסונים שכבר נמצאים בשימוש – מתמקדים בחלבון ה"ספייק" (spike) – אותו חלבון ידוע לשמצה הנמצא על מעטפת הנגיף ומקנה לו את צורת הכתר המפורסמת שלו. ואולם ידוע כיום כי חלבון זה נוטה לפתח מוטציות אשר שוחקות את יעילות הטיפולים השונים. "מכיוון שהנגיף משתנה ללא הרף, החלטנו שיהיה נכון יותר להתמקד בחלבון שאינו משתנה – הקולטן ACE2 שבאמצעותו נכנס הנגיף לתאי הגוף שלנו", מסביר פרופ' גדעון שרייבר מהמחלקה למדעים ביומולקולריים במכון ויצמן. גישה טיפולית זו צפויה להיות עמידה יותר בפני הופעת וריאנטים חדשים של הנגיף – האתגר המרכזי הניצב כיום בפני מיגור המגיפה.

הקולטן ACE2 אשר נמצא על קרומי תאים המרפדים את דפנות הריאה (ומכאן הפגיעה הידועה של הקורונה באיבר זה) ואיברים נוספים, הוא אנזים חיוני המשתתף בתהליכי בקרת לחץ דם. לפיכך, מפתה ככל שזה יהיה, לא מומלץ לפתח תרופה שתחסום את פעילותו לאלתר. בהתאם לכך, מעבדתו של פרופ' שרייבר, המתמחה בחקר קשרי גומלין בין חלבונים, שמה לה למטרה לפתח מולקולת חלבון שתיקשר ל-ACE2 בצורה טובה ויעילה יותר מאשר חלבון הכתר הנגיפי – ובכך תחסום את דרכו של הנגיף מלחדור לתאים – מבלי לשבש את פעילותו החיונית של הקולטן.
בעודם סורקים את מיליוני המוטציות שהתקבלו, גילו החוקרים דבר מדהים: כבר אחרי הסבב האבולוציוני הראשון, נוצרו במעבדה מוטציות שחזו את התפתחותם של וריאנטים מדבקים יותר של נגיף הקורונה – הזן הבריטי (אלפא), הדרום-אפריקאי (בטא) והברזילאי (גמא)
המדענים, בהובלת החוקר הבתר-דוקטוריאלי ד"ר יריי זהארדניק, בודדו את אתר הקישור ל-ACE2 על גבי חלבון הכתר – והעבירו אותו סדרת סבבים של "אבולוציה במבחנה". שיטה זו, ששוכללה על-ידי ד"ר יריי זהארדניק, ומדמה את תהליכי הברירה הטבעית רק בהילוך מהיר בהרבה, עושה שימוש בזן מהונדס גנטית של שמר האפייה. מכיוון שתאי שמרים הם מצע נוח לשינויים גנטיים, יכלו החוקרים לסרוק ביעילות ובמהירות מיליוני מוטציות שנוצרו בתאי השמרים במהלך סבבי הברירה המלאכותית. "המטרה הסופית הייתה למצוא מולקולה שתהיה 'דביקה' באופן משמעותי יותר מהגרסה הנגיפית המקורית ובכך לחסום את שער הכניסה " אומר פרופ' שרייבר.
בעודם סורקים את מיליוני המוטציות שהתקבלו, גילו החוקרים דבר מדהים: כבר אחרי הסבב האבולוציוני הראשון, נוצרו במעבדה מוטציות שחזו את התפתחותם של וריאנטים מדבקים יותר של נגיף הקורונה – הזן הבריטי (אלפא), הדרום-אפריקאי (בטא) והברזילאי (גמא). עובדה זו מצביעה בבירור על הקשר בין עוצמת הקשירה לקולטן ACE2 ומידת היעילות של הנגיף. מעניין שדווקא המוטציות המאפיינות את הזן ההודי (דלתא), הזן הדומיננטי כיום במקומות רבים בעולם, לא הופיעו בניסוי בתאי השמרים, שכן המוטציות שהפכו את הדלתא למדבק כל כך שיפרו בעיקר את יכולתו לחמוק מפני המערכת החיסונית – ולא את יכולתו להיקשר ל-ACE2.
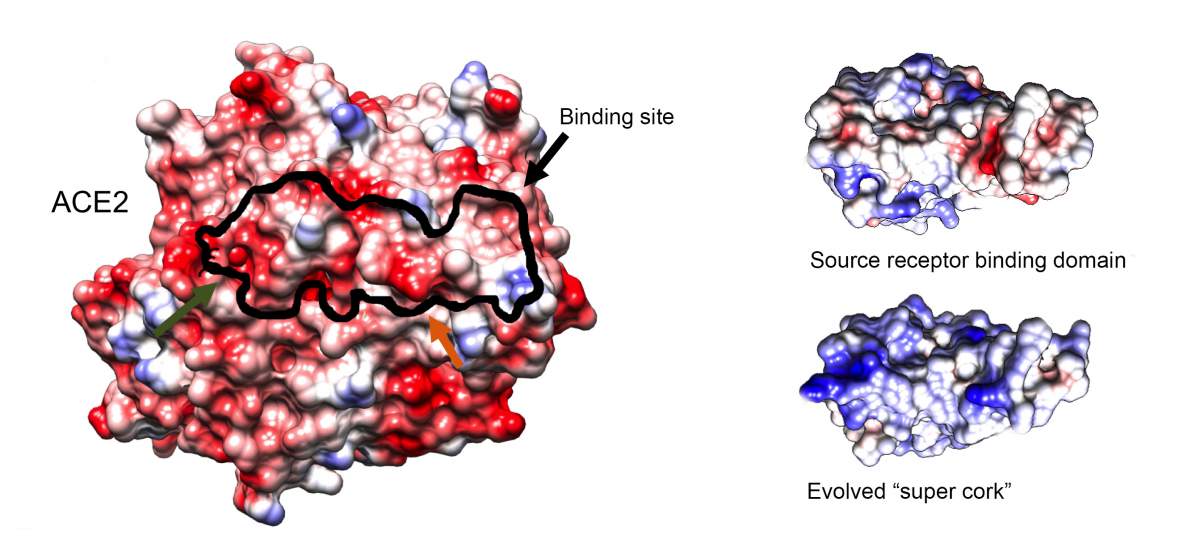
מבין מיליוני המוטציות שנוצרו, בודדו החוקרים מולקולת חלבון קטנה שיכולת ההיקשרות שלה לקולטן ACE2 גבוהה פי 1,000 מאשר יכולת ההיקשרות של אתר הקישור המקורי של הנגיף. בנוסף, תלמידות המחקר מאיה שמש ושיר מרציאנו הראו כי לא רק שחלבון זה מתאים ל-ACE2 כמו פקק לבקבוק, הוא גם אינו פוגע כלל בתפקוד החיוני של ACE2. יותר מכך, הודות ליכולת ההיקשרות העוצמתית שלו, נדרשו ריכוזים נמוכים ביותר ממנו בכדי "לפקוק" את שער הכניסה של הנגיף ולחסום את דרכו. זאת ועוד, כפי שחזו המדענים, הפקק פעל באותה יעילות נגד כל סוגי הווריאנטים המוכרים של הנגיף.
בכדי להפוך את מולקולת הפקק לתרופה פוטנציאלית לקורונה, חברו במעבדתו של פרופ' שרייבר לפרופ' ינון רודיך מהמחלקה למדעי כדור-הארץ וכוכבי-הלכת במכון, ופיתחו – בשיתוף עם ד"ר אירה מרטון וד"ר צ'יונלין לי – שיטה למתן החלבון לחולים באמצעות תרסיס נשימתי. גישה טיפולית חדשה זו נבדקה בהצלחה בניסוי באוגרים ב-NIH – הטיפול הפחית באופן משמעותי את הופעת התסמינים ואת עוצמתם. מחקרים טרום-קליניים נוספים צפויים להתקיים ב-NIH בעתיד הקרוב.
בעודם מחפשים אחר "פקק-על" שיחסום את קולטן ה-ACE2, סרקו המדענים כ-1,000,000,000 מוטציות של תאי שמרים.
לקבלת מידע נוסף, תמונות ולתיאום ראיונות:
משרד הדוברת - מכון ויצמן למדע
08-9343856 news@weizmann.ac.il