עיתונאיות ועיתונאים, הירשמו כאן להודעות לעיתונות שלנו
הירשמו לניוזלטר החודשי שלנו:
נהוג לומר שהבגד עושה את האדם, והדבר נכון גם לגבי החלבונים בגופנו, אשר בתגובה לשינויים סביבתיים ותוך-תאיים עוטים על עצמם תגיות כימיות המשנות אותם לבלי היכר. מלתחה של מאות תגיות שונות מסייעת לאלפי החלבונים בגופנו לבצע את שלל משימותיהם החשובות, אך מקשה על מדענים ורופאים לזהות מולקולות חיוניות אלה. מעבדתה של פרופ' יפעת מרבל במכון ויצמן למדע הציבה לעצמה אתגר: להצליח לזהות בבת אחת מספר גדול ככל האפשר של חלבונים – על שלל תלבושותיהם השונות.
ממש כמו חבישת כתר או עטיית גלימה של גיבור-על, הצמדת תגית כימית מחוללת מהפך בחייו של חלבון: בכוחן של תגיות אלה לשנות את כל תכונותיו הבסיסיות – מיציבותו ומיקומו בתא ועד יכולות הקישור שלו למולקולות אחרות. כדי להגיע להבנה מעמיקה יותר של תהליכים גופניים שונים ושל התפתחות מחלות ואף פיתוח טיפולים חדשניים, נדרש מאיתנו לזהות את החלבונים גם כאשר הם בשינוי אדרת. מידע זה עשוי, למשל, לאפשר לזהות חלבונים עם תגיות שהן ספציפיות לתאים סרטניים וכך לחשוף את התאים האלה ולהשמידם. תלבושות לא תקניות עשויות להסביר גם התפתחות מחלות אוטואימוניות, שבהן הגוף תוקף את רקמותיו שלו עצמו, ואולי אף להוביל לטיפולים חדשים במחלות אלה.

אבל זיהוי החלבונים על תגיותיהם הוא מלאכה מאתגרת במיוחד. גנום האדם מכיל כ-20 אלף גנים מקודדי חלבונים, וכל אחד מהם יכול לייצר ארבע או חמש גרסאות חלבון, כלומר, ישנם כ-100 אלף רצפים חלבוניים שונים בגופנו. כל אחד מחלבונים אלה, לאחר שכבר נוצר, יכול לעבור שינוי כימי באמצעות תגית אחת או יותר, מתוך מבחר של יותר מ-200 תגיות. אם נוסיף לכך את העובדה שתגיות יכולות להיצמד למקומות שונים על-גבי החלבון, נקבל מספר כמעט אינסופי של צירופי תיוג שונים.
ממש כמו חבישת כתר או עטיית גלימה של גיבור-על, הצמדת תגית כימית מחוללת מהפך בחייו של חלבון: בכוחן של תגיות אלה לשנות את כל תכונותיו הבסיסיות מיציבותו ומיקומו בתא ועד יכולות הקישור שלו למולקולות אחרות
השיטות המקובלות כיום לזיהוי חלבונים בדגימה אינן מאפשרות לזהות את החלבונים המתויגים: לכל חלבון יש רצף ייחודי של חומצות אמינו, אבני הבניין של החלבונים, אך התגיות מפריעות לזיהוי, שכן הן משנות את התכונות של חומצות האמינו. עד כה היה קשה לאתר ביעילות שינויים כימיים המתרחשים בחלבונים לאחר היווצרותם, ומרבית המחקרים התמקדו במספר מצומצם בלבד של שינויים בחלבונים. "על מנת להבין תהליכים ביולוגיים במלוא מורכבותם, חייבים לחקור את ההשפעות של התגיות המוצמדות לחלבונים", מסבירה פרופ' מרבל מהמחלקה לאימונולוגיה מערכתית של המכון. "המעבדה שלי שמה לה למטרה ליצור שיטה חישובית חדשה המסוגלת לאתר עשרות סוגי תיוג של חלבונים בו-בזמן".

מנוע החיפוש אשר פותח על-ידי פרופ' מרבל וחברי קבוצתה מכוון לאיתורן של תגיות רבות במקביל, במקום להתמקד כל פעם בתגית אחת בלבד כפי שנעשה בעבר. השיטה נקראת באנגלית PROMISE, ראשי תיבות של Protein Modification Integrated Search Engine, ונראה כי היא עומדת בציפיות המשתמעות משמה: מנוע החיפוש מאפשר לזהות כ-30 תגיות בתוך שש שעות, לעומת שלוש תגיות בלבד בתוך שבועיים בשיטות הקיימות. הפיתוח נעשה בהובלה של אסף קסן, בשיתוף עם אהרון ג'ביט; שניהם היו תלמידי מחקר במעבדתה של פרופ' מרבל.
"PROMISE מספקת לנו משקפיים חדשים המאפשרים להביט על תהליכים ביולוגיים ברזולוציה גבוהה יותר מאי פעם", אומרת פרופ' מרבל. "כלי זה יאפשר, בין היתר, לבחון מחדש סוגיות ביו-רפואיות לא פתורות באמצעות הנתונים קיימים".
קסן, ג'ביט ועמיתיהם למחקר הדגימו את ביצועיו של מנוע החיפוש באמצעות שאלה בסיסית בחקר הסרטן: כיצד משפיע תיוג חלבונים על יכולתה של המערכת החיסונית לזהות גידולים ולחסלם. החוקרים בדקו באמצעות PROMISE מאות מקטעי חלבון (פפטידים) מתוך יותר מ-200 דגימות של תאים ורקמות הקשורים לסרטן. הם התמקדו בעיקר בפפטידים המוצגים על-גבי המעטפת של תאים סרטניים, וכך עשויים לאותת למערכת החיסונית כי התא ממאיר ויש לחסלו.
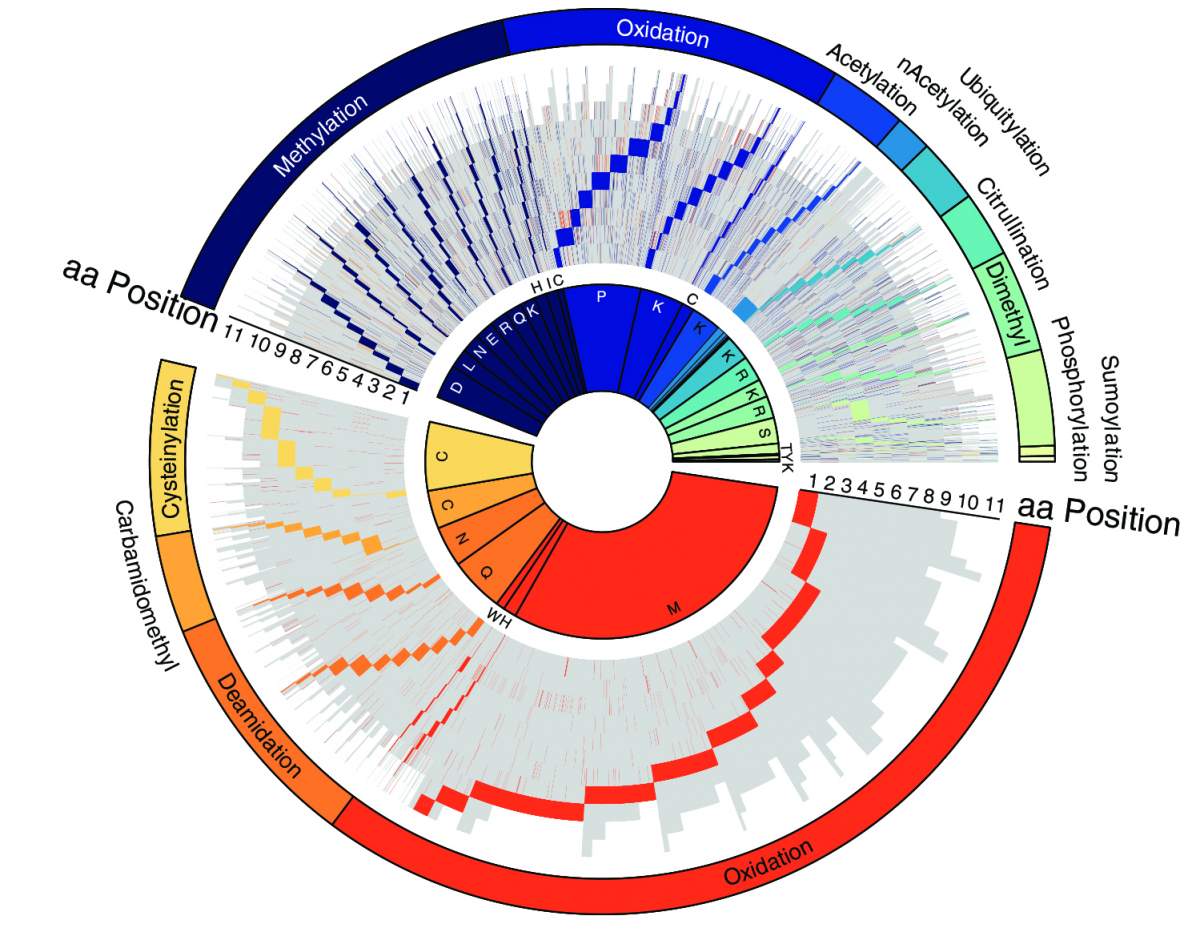
המדענים בדקו כ-30 שילובים של תגיות והצליחו לזהות תת-קבוצה של כ-12 אלף פפטידים מתויגים, שלא זוהו בעבר בשיטות חישוביות אחרות. התוצאה היא האטלס המקיף ביותר עד כה של פפטידים המאפיינים גידולים סרטניים וכן מקרא מיוחד המראה כיצד מיקומן של התגיות משפיע על יכולתה של המערכת החיסונית לזהות את התא הסרטני. זהו מידע חיוני, שכן חלק מהתגיות עשויות להסביר כיצד עוטה תא סרטני "גלימה" המסתירה אותו מפני תאי T של המערכת החיסונית. בהמשך אפשר אולי יהיה ללמוד לקרוע מעליו את הגלימה ובכך לשפר את הטיפולים האימונותרפיים הקיימים – טיפולים אשר רותמים את תאי T של המערכת החיסונית למלחמה בסרטן.
מלבד סרטן, ייתכן כי בעתיד אפשר יהיה להשתמש ב-PROMISE גם במחלות אוטואימוניות – לחשוף מקטעי חלבון מתויגים אשר מבלבלים את תאי המערכת החיסונית שלנו וגורמים להם לתקוף תאים בריאים. השיטה עשויה להוביל גם לתובנות חדשות בנוגע למחלות מוח ניווניות ומחלות נוספות. "זיהוי מהיר של תגיות חלבון עשוי לעזור בזיהוי תהליכי מחלה רבים וכמו כן, לאפשר לנו לבחון את יעילותן של תרופות ואף לפתח תרופות חדשות", אומרת פרופ' מרבל.
במחקר השתתפו ד"ר מתיאס קרמר וד"ר מרב שמואלי מהמחלקה לאימונולוגיה מערכתית של המכון; ד"ר דוד מורגנשטרן וד"ר ישי לוין מהמרכז הישראלי הלאומי לרפואה מותאמת אישית על-שם ננסי וסטיבן גרנד; תומר צבן ופרופ' אורה שולר-פורמן מהאוניברסיטה העברית בירושלים; ד"ר גואו סי תאו, ד"ר פליפה דה וייגה לפרבוסט, ד"ר פנגצ'או יו ופרופ' אלקסיי נסביז'סקי מאוניברסיטת מישיגן; ד"ר אילון ברנע ופרופ' אריה אדמון מהטכניון; פרופ' לאה איזנבך מהמחלקה לאימונולוגיה וביולוגיה רגנרטיבית של המכון; ופרופ' ירדנה סמואלס מהמחלקה לביולוגיה מולקולרית של התא של המכון.
יותר מ-10% מהחלבונים המיוצרים על-ידי הגנום האנושי הם אנזימים המצמידים תגיות לחלבונים אחרים. שיטות אנליטיות סטנדרטיות שאינן מביאות בחשבון תגיות או מוטציות – מזהות רק 50% עד 80% ממקטעי החלבון בדגימות ביולוגיות. במלים אחרות, בכל דגימת רקמה, עד 50% מהרצפים החלבוניים נותרים לא מזוהים.