עיתונאיות ועיתונאים, הירשמו כאן להודעות לעיתונות שלנו
הירשמו לניוזלטר החודשי שלנו:
תצפית מפתיעה במוח של דג זברה הובילה את מדעני מכון ויצמן למדע לקרוא תיגר על דוקטרינה בת 200 שנה בדבר מוצאו של איבר קטן וחיוני ביותר במוחנו – בלוטת יותרת המוח או בשמו הלטיני היפופיזה. ממצאי המחקר, אשר נערך במעבדתו של פרופ' גיל לבקוביץ, עשויים לתרום להבנה חדשה של יחסי הגומלין בין תאים שונים, ובהם תאים מפרישי הורמונים, בבלוטה זו, ולהאיר אור חדש על מחלות שבהן היא מעורבת.
ההיפופיזה ממוקמת בבסיס המוח, גודלה כגודל אפון בבני אדם, והיא מעין "תחנת ממסר" של מערכת הפרשת הורמונים מהמוח אל הגוף. הבלוטה נשתמרה היטב לאורך האבולוציה – ועל כן, זו שברשותנו חולקת מאפיינים רבים עם אלו של מגוון בעלי-חיים אחרים, קרובים כרחוקים. הבלוטה מורכבת משתי אונות נפרדות, וכל אחת משרתת תפקידים פיזיולוגיים שונים: זו הקדמית משחררת לזרם הדם שישה הורמונים עיקריים, ובהם הורמוני בלוטת התריס והורמוני גדילה, בעוד האונה האחורית משחררת שניים בולטים – ואזופרסין המווסת את רמת המלחים וכמות הנוזלים בגוף, ואוקסיטוצין המווסת רבייה והתנהגות חברתית.

שאלת המקור העוברי של ההיפופיזה העסיקה מדענים כבר בתחילת המאה ה-19. בראשית התפתחותו, מורכב העובר משלוש שכבות נבט – קבוצות התאים העיקריות שמתוכן נוצרות רקמות הגוף כולן; השכבה הפנימית נקראת אנדודרם, האמצעית מזודרם, והחיצונית אקטודרם. שכבה חיצונית זו, מחולקת בתורה לשניים: האקטודרם האוראלי, שממנו מתפתחים בין היתר העור, חלל הפה, השיניים והעיניים, והאקטודרם העצבי שממנו מתפתחים המוח וחלקים ממערכת העצבים. עד כה, התיאוריה המקובלת הייתה שהמקור התאי של שתי אונות ההיפופיזה הוא באקטודרם, כאשר האונה הקדמית מקורה בתאי האקטודרם האוראלי, בעוד האחורית מוצאה באקטודרם העצבי. רעיון זה הוצג לראשונה בשנת 1838 על ידי האמבריולוג הגרמני מרטין רתקה (Rathke), והוא קיבל תמיכה במחקרים רבים לאחר מכן.
""הממצא שלנו סתר את הרעיון שלשתי אונות ההיפופיזה יש מקורות נפרדים לחלוטין. היו לכך רמזים במחקרים קודמים, אבל לא הוצג האקדח המעשן"
צ'יו צ'ן, דוקטורנטית במעבדתו של פרופ' לבקוביץ במחלקה לביולוגיה מולקולרית והמחלקה למדעי המוח המולקולריים במכון, עסקה במיפוי גנטי של האונה הקדמית של ההיפופיזה בדגי זברה. בעזרת שיטות דימות ושיטות גנטיות חדישות אשר לא היו זמינות לחוקרים בעבר, צ'ן הצליחה לסמן תאים שונים ברקמה האקטודרמלית של עובר דג הזברה, וכך לעקוב תחת מיקרוסקופ אחר התאים השונים שנוצרו מתוך תאים אלו במהלך התפתחות העובר והיווצרות בלוטת יותרת המוח. בהתאם לתיאוריה המקובלת, ציפתה צ'ן לראות באונה הקדמית אך ורק תאים עם סימונים גנטיים שמקורם באקטודרם האוראלי. למרבה ההפתעה, המוצא של חלקם היה דווקא באקטודרם העצבי.
"ממצא זה סתר את הרעיון שלשתי אונות ההיפופיזה יש מקורות נפרדים לחלוטין", אומר פרופ' לבקוביץ. "היו לכך אמנם רמזים במחקרים קודמים, אבל עד כה לא הוצג האקדח המעשן שיהווה הוכחה חותכת לסטייה מהתיאוריה הרווחת".
"האקדח המעשן" במחקר הנוכחי הוא למעשה תאים שהתגלו באונה הלא נכונה לכאורה. הממצאים התאפשרו בעזרת שילוב בין המעקב הגנטי שהפעילה צ'ן ובין שיטות מתקדמות לריצוף החומר הגנטי ברמת התא הבודד שיושמו בשיתוף פעולה עם מעבדתו של פרופ' עידו עמית מהמחלקה לאימונולוגיה מערכתית במכון. בעזרת שילוב השיטות, הצליחו המדענים לפענח את ההרכב המולקולרי המדויק של רקמת ההיפופיזה ברמת התא הבודד ולעקוב אחר התפתחותה בעוברי דג זברה.
עם התקדמות המחקר, נודע למדעני המכון כי חוקרת במכון פרנסיס קריק בלונדון, ד"ר קארין ריזוטי, נתקלה בממצא דומה בעכברים. "היא היתה סקפטית לגבי הממצאים, אבל שיתפנו אותה שהגענו לממצאים דומים בדגים והזמנו אותה לשתף פעולה ולאחד כוחות, כדי לייצר 'קייס' חזק יותר", מספר פרופ' לבקוביץ.
מלבד שבירת הדוקטרינה, מיפוי סוגי התאים המרכזיים ביותרת המוח הוביל לממצא מפתיע נוסף: דו-שיח בין שתי האונות. החוקרים גילו שתאים מסוימים באונה האחורית הקרויים פיטוציטים משפיעים על התפתחותם של תאים מייצרי הורמונים באונה הקדמית. "ידענו שפיטוציטים מעורבים בשחרור ואזופרסין ואוקסיטוצין מהאונה האחורית, כעת מתברר שהם גם ממלאים תפקיד בהתפתחות יותרת המוח הקדמית", אומרת צ'ן.
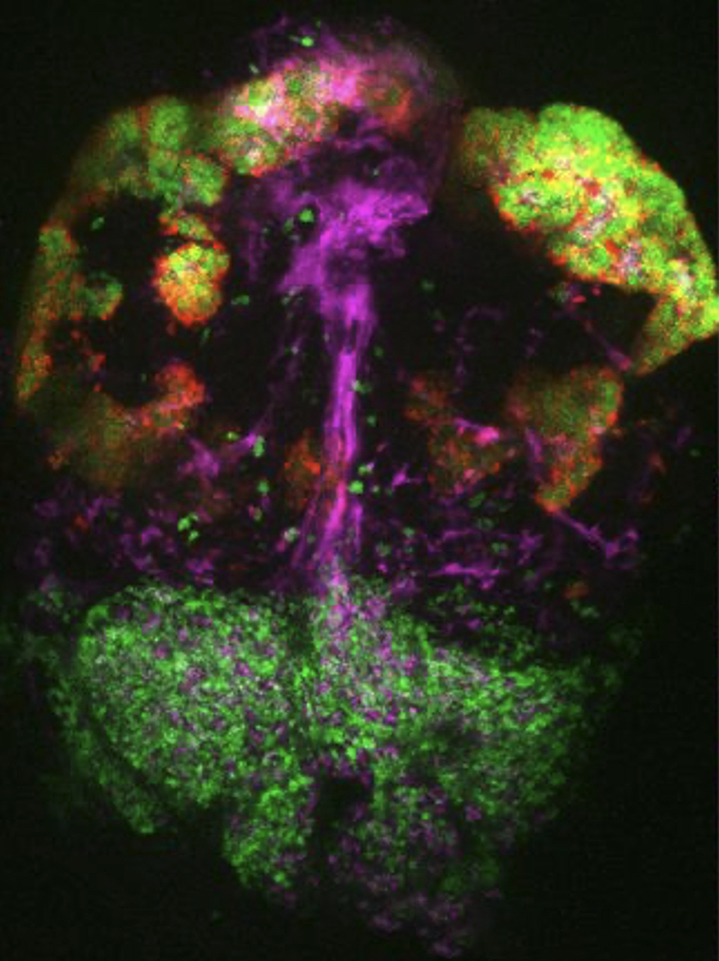
"על האנטומיה של בלוטת יותרת המוח יש לנו ידע רב, אבל בכל הנוגע להבנת ההרכב המולקולרי שלה הדרך עוד ארוכה", אומר פרופ' לבקוביץ. "הבנה של ההבדלים הגנטיים בין התאים השונים, כיצד הבדלים אלה נוצרים בשלבים מוקדמים של התפתחות העובר, ואיך סוגי התאים השונים משפיעים זה על זה – עשויים לעזור לנו להבין מה משתבש במחלות שונות שבהן מעורבת יותרת המוח, ובכלל זאת סוגי סרטן שונים ומחלות ילדים מסוימות, כמו למשל מחסור בהורמון גדילה".
למרות הגילויים החדשים, מציין פרופ' לבקוביץ כי הדוקטרינה בנוגע למקורות הנפרדים של שתי האונות עדיין נכונה ברובה, אך המחקר הנוכחי מציג תמונה מורכבת יותר שעשויה להוביל לדרכים חדשות לחקר שיבושים בפעילות יותרת המוח. צ'ן מסבירה: "נניח שיש לך 100 תאי הורמון גדילה. 95 מהם מוצאם אכן באקטודרם האוראלי, כפי שנהוג היה לחשוב. אבל כעת מתברר, שהמקור של חמישה הוא דווקא עצבי. כל מאה התאים האלו משחררים אותו הורמון – אבל אולי הם עושים זאת בתגובה לדרישות פיזיולוגיות שונות? הבנה זו עשויה לפתוח אפשרויות לטיפול במחלות הנובעות מחוסרים הורמונליים באמצעות התמקדות בתאים ספציפיים, ותוך הימנעות מהשפעה לא רצויה על תאים אחרים".
במחקר השתתפו גם ד"ר דינה לשקוביץ מהמחלקה לתשתיות מחקר מדעי החיים של המכון; ד"ר האנג'י לי; ד"ר אנדריאס ואן אימפל; ופרופ' סטפן שולטה-מרקר מאוניברסיטת מינסטר, מינסטר, גרמניה.
מחסור משולב בהורמוני יותרת המוח (CPHD) הוא מצב רפואי הגורם למחסור ב-2 הורמונים או יותר המיוצרים בהיפופיזה. לפי הערכות, מצב זה מאפיין 1 מ-8,000 אנשים ברחבי העולם.