עיתונאיות ועיתונאים, הירשמו כאן להודעות לעיתונות שלנו
הירשמו לניוזלטר החודשי שלנו:
אנחנו שוחים בעולמות שונים, אבל בני-אדם ודגים קרובים מכפי שנראה לעין. דמיון ביולוגי מפתיע זה אפשר לצוות מחקר ממכון ויצמן למדע ומהמרכז הרפואי שיבא (תל-השומר) למצוא טיפול מבטיח למחלה מסכנת חיים של מערכת הלימפה בעזרתם של דגיגי זברה. המחקר המשותף יצא לדרך לאחר שלמרפאתה של פרופ' שושנה גרינברגר בבית-החולים ספרא לילדים בשיבא הגיע ילד בן תשע עם בעיות נשימה חמורות. כשאובחן עם מחלה גנטית נדירה המכונה kaposiform lymphangiomatosis או בקיצור KLA, פנתה הרופאה למעבדתה של פרופ' קרינה יניב במכון ויצמן החוקרת כבר יותר משני עשורים את היווצרותם של כלי הדם וכלי הלימפה באמצעות דגי זברה. למרבה הצער, שיתוף הפעולה לא הספיק להציל את הילד, אך הוביל בסופו של דבר לגילוי שתי תרופות פוטנציאליות למחלה חשוכת המרפא. ממצאים מעוררי תקווה אלה מתפרסמים כעת בכתב-העת הרפואי Journal of Experimental Medicine.

סימן ההיכר של KLA הוא כלי לימפה מוגדלים ומעוותים שאין ביכולתם לבצע את מלאכתם כהלכה: לנקז נוזלים מרקמות הגוף ולתמוך בשלל תפקודים חיוניים. כמו במקרה של הילד שהגיע למרפאתה של פרופ' גרינברגר, החולים מאובחנים לרוב בגיל צעיר עקב קשיי נשימה הנובעים מהצטברות נוזלים בבית החזה, אך המחלה פוגעת גם בעור ובאיברים רבים אחרים.
במחקר קודם שהובילה, זיהתה פרופ' גרינברגר מוטציה בגן NRAS המובילה למחלה. מכיוון שגן זה ידוע כאונקוגן, כלומר גן שמוטציה בו עלולה להוביל להתפתחות סרטן, החלו רופאים ברחבי העולם לטפל בחולי KLA בתרופות נגד סרטן החוסמות את NRAS או את החלבונים הקשורים אליו. ואולם ההצלחה של טיפולים אלה היא חלקית בלבד, והם כרוכים גם בתופעות לוואי קשות.
""זה היה רגע מדהים. כשראיתי את הדגים המהונדסים, מיד ידעתי שאנחנו בדרך הנכונה"
"פנינו לפרופ' יניב, כי רצינו לוודא שהמוטציה שמצאנו היא אכן זו שמחוללת את המחלה, וגם להבין טוב יותר את המנגנון מאחורי התפתחותה בתקווה למצוא טיפול טוב יותר", מסבירה פרופ' גרינברגר, העומדת בראש המרכז הרב-תחומי לאנומליות וסקולריות בשיבא.
את צוות המחקר המדעי-רפואי שהתגבש הובילו במשותף פרופ' גרינברגר משיבא ופרופ' יניב והוא כלל גם את ד"ר איוון באסי, חוקר בתר-דוקטוריאלי במעבדתה של פרופ' יניב במחלקה לאימונולוגיה ורגרנציה ביולוגית במכון. החוקרים החליטו לקפוץ למים ולפתח מודל של מחלת KLA אנושית בדגי זברה. מכיוון שמערכת הלימפה של דגים אלה דומה מבחינות רבות לזו של בני-אדם, החל מההרכב הגנטי וכלה במבנה האנטומי, ולאור העובדה שהגן NRAS האנושי זהה בכ-80% לגרסתו בדגי זברה, יכלו החוקרים להחדיר לעוברי הדגים הזעירים את הגן הפגום שהוצא מתאיו של המטופל הצעיר. אבל האתגר היה לוודא שהגן מתבטא אך ורק בכלי הלימפה של הדגיגים, כמו במחלה האנושית, ולא בשום מקום אחר בגוף; את הבדיקות שנועדו לוודא את תקפות המודל הובילה אמאני גבאלי, סטודנטית לתואר שני בהנחיית פרופ' גרינברגר ופרופ' יניב.

בסופו של דבר העוברים המהונדסים עם הגן האנושי הפגום פיתחו את המאפיינים המרכזיים של KLA בבני-אדם, הכוללים כלי לימפה מוגדלים ונפיחות סביב הלב. "זה היה רגע מדהים", משחזרת פרופ' יניב. "כשראיתי את הדגים המהונדסים, מיד ידעתי שאנחנו בדרך הנכונה".
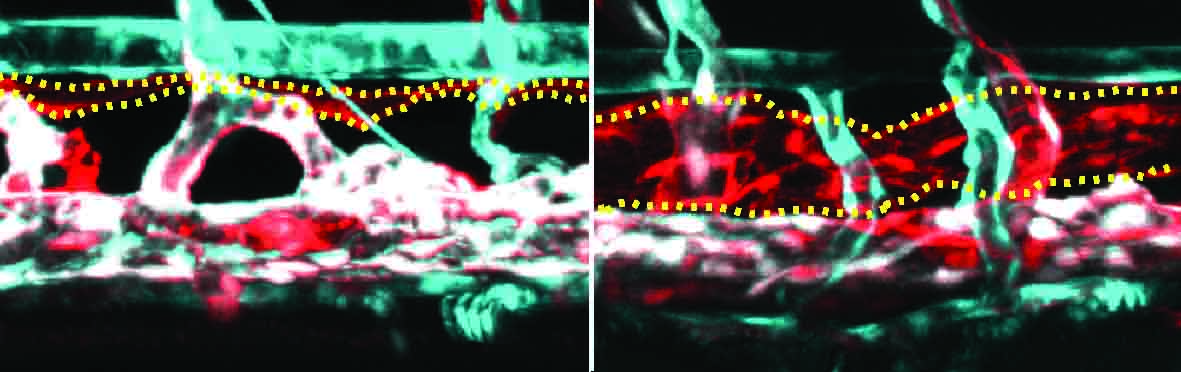
באמצעות המודל הדגיגי, פיענחו ד"ר באסי ועמיתיו את פרטי המנגנון של המחלה שלא היו ידועים עד כה. בגרסתו התקינה, NRAS מורה לתאים להתחלק בכפוף לקבלת אות הפעלה, אך החוקרים גילו כי המוטציה גורמת לכך שהגן נותר במצב "פעיל", ולכן התאים של כלי הלימפה מתחלקים וצומחים ללא בקרה.
השלב המכריע הבא היה למצוא מולקולה קטנה שתוכל לבלום את ההשפעה ההרסנית של המוטציה. עוברים מהונדסים של דגי זברה הם מועמדים מושלמים למשימה זו – הם שקופים ומאפשרים לבחון פעילות של תרופה אפשרית, לא רק בחלבונים או בתאים בודדים, אלא ביצור חי שלם – אבל הדגיגים הזעירים יצרו גם כאב ראש לא קטן. סריקה בתפוקה גבוההhigh-throughput screening) ), השיטה הסטנדרטית לבדיקה מהירה של מספר רב של תרופות פוטנציאליות, נעשית בדרך כלל באמצעות מכונות, והחוקרים נתקלו בבעיה חלקלקה במיוחד: כיצד להניח כל עובר של דג זברה תחת מיקרוסקופ בדיוק אותה הדרך – מבלי לעשות זאת ידנית – כך שהמכונה תוכל לצלם את כל העוברים באופן אחיד ולהעריך כהלכה את השפעת התרכובות השונות?
הצוות, בעזרת ציוד מעבדה ייחודי שנרכש מחברה יפנית, פיתח שיטה חכמה, המאפשרת להפיל כל דגיג בעדינות, באופן ממוכן ואחיד, לתוך חריץ תחת המיקרוסקופ. לאחר מכן אלגוריתם AI עיבד את התצלומים המיקרוסקופיים, וחישב את ההיקף ואת שטח הפנים של הדגיגים לאחר החשיפה לתרופה פוטנציאלית. מכיוון שבדגים המהונדסים הלב היה מוגדל, חשיפה לתרופה יעילה אמורה הייתה להיתרגם לצמצום בשטח הפנים שלהם. כך בדקו החוקרים יותר מ-150 מולקולות קטנות – כולן תרופות שכבר אושרו לשימוש במחלות אחרות. כ-30 מהן הראו תוצאות מבטיחות, ובבדיקות שנערכו בהמשך נבחרו שתיים שהיו היעילות ביותר.
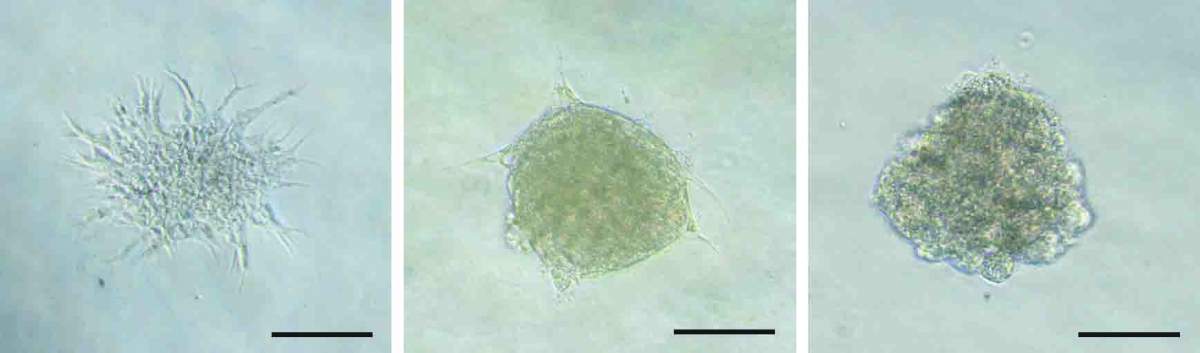
שתי התרופות ביטלו את התסמינים של KLA במודל של דגי זברה. הלב המנופח וכלי הלימפה העיקרי המוגדל חזרו לצורתם ולממדיהם הרגילים. כדי לבדוק האם תרופות אלה עשויות לטפל במחלה בבני-אדם, בחנו החוקרים את השפעתן על תאי הלימפה של הילד שטופל על ידי פרופ' גרינברגר. התוצאה הייתה ניכרת: שתי התרופות חסמו את צמיחת השלוחות בתאי הלימפה, תופעה לא תקינה המאפיינת KLA. אם נוסיף לכך ששתיהן נחשבות לבטוחות יותר מאשר התרופות שבהן משתמשים כיום רופאים לטיפול ב-KLA, וכי הן אמורות לגרום לתופעות לוואי מופחתות, מדובר במועמדות מבטיחות במיוחד.
"אנחנו מקווים שבקרוב ייערך ניסוי קליני כדי לבדוק את השפעתן של תרופות אלה בחולים", אומרת פרופ' גרינברגר. "KLA היא מחלה נדירה, ונפעל ליצירת שיתוף פעולה בינלאומי בין כמה מרכזים רפואיים כדי לגייס לניסוי מספיק משתתפים".
בינתיים ממשיכה מעבדתה של פרופ' יניב להשתמש במודל בדגים כדי לחקור מחלות אחרות של מערכת הלימפה וגם להעמיק את ההבנה של KLA. "תעלומה אחת עומדת בעינה: למה המוטציה ב-NRAS הפוגעת באופן כל כך חמור במערכת הלימפה לא משפיעה כלל על מערכת הדם?", שואלת פרופ' יניב. "אבל אלה שאלות לטווח ארוך יותר. מה שמצאנו במחקר הנוכחי עשוי לעזור לחולים עוד קודם לכן, שכן התרופות שזיהינו כיעילות כבר אושרו למחלות אחרות. לקבל אישור להתוויה חדשה לתרופות מאושרות, זה תהליך מהיר בהרבה מאשר להתחיל מאפס".
במחקר השתתפו גם ג'וזפינה למביאסה, נגה משה, ד"ר יערה טבת, גל פרלמוטר, שני אגוזי וג'ונתן לונג מהמחלקה לאימונולוגיה ורגנרציה ביולוגית של המכון; ד"ר לוטן לוין, נעמה פרג', ד"ר גיל ש. לייכנר, ד"ר פולינה גבע, פרופ' אביב ברזילי וד"ר קמילה אביבי מהמרכז הרפואי שיבא; ד"ר ג'ייסון אוטרסטרום וד"ר יעל פארן מ IDEA Bio-Medical Ltd, רחובות; וד"ר חיים בר מהמרכז הישראלי הלאומי לרפואה מותאמת אישית ע"ש ננסי וסטיבן גרנד.
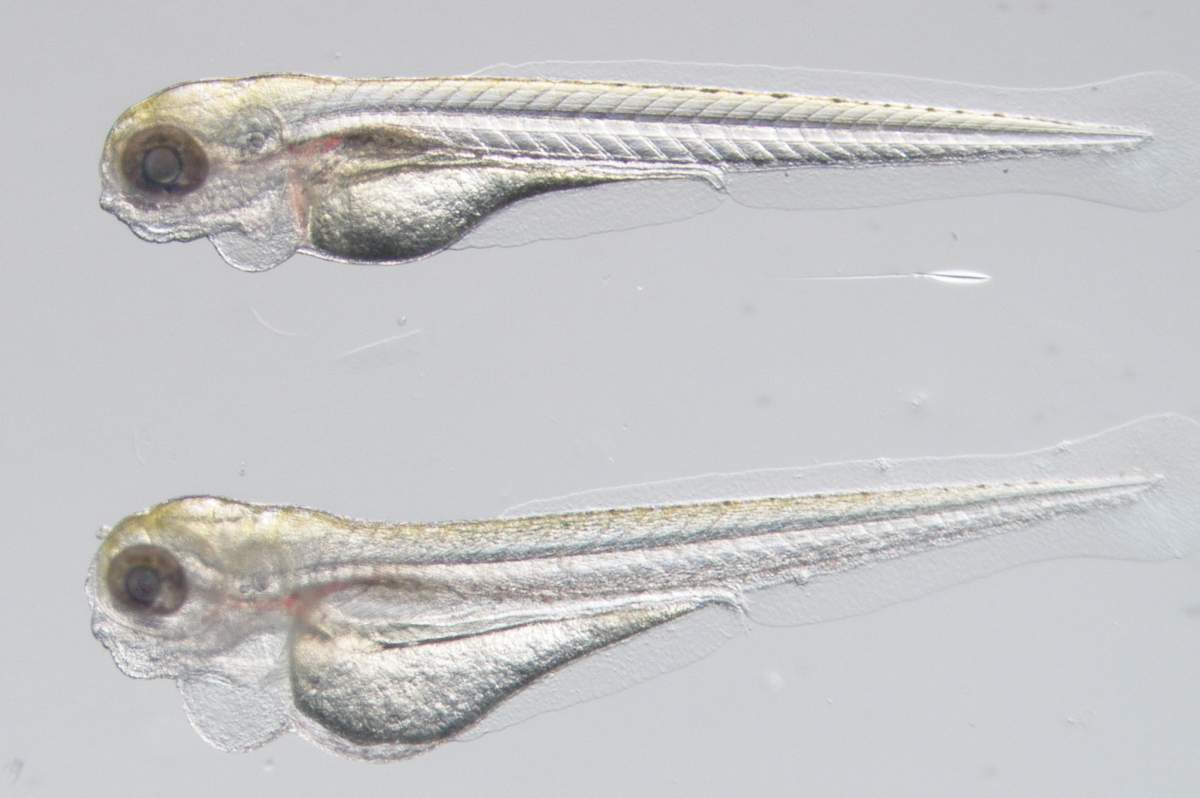
עוברי דג זברה ששימשו כמודל למחלת KLA הגיעו לאורך של כ-4 מילימטרים בגיל 5 ימים.