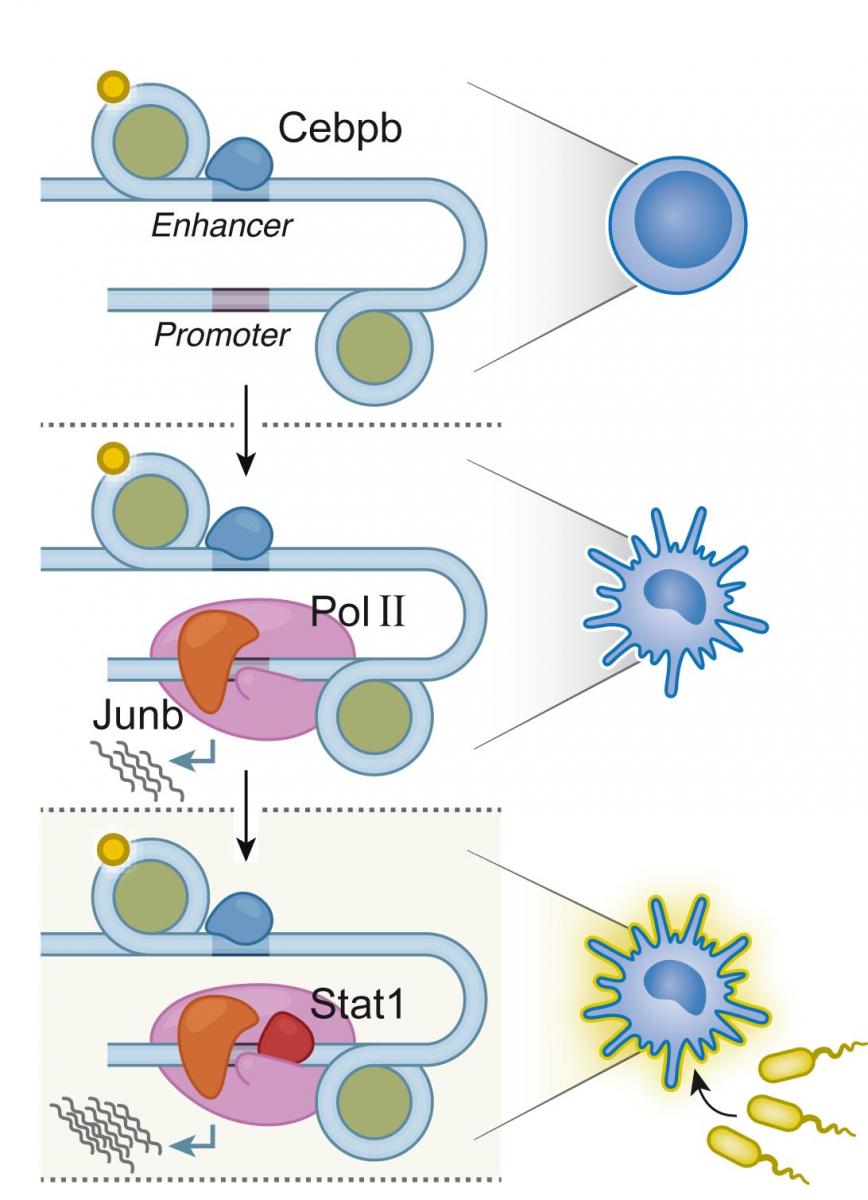
על אף חשיבותם הרבה, מנגנוני הפעילות של גורמי הבקרה עדיין אינם מובנים. כעת הצליח צוות מדענים, בראשותו של
ד"ר עידו עמית מהמחלקה לאימונולוגיה במכון ויצמן למדע, בשיתוף עם מדענים ממכון Broad שבמסצ'וסטס, וביניהם מנואל גרבר וניר יוסף, וכן אביב רגב וניר פרידמן מהאוניברסיטה העברית, לפתח שיטה מתקדמת לסריקה ולמיפוי שלהם. ממצאי המחקר,
שהתפרסמו בכתב- העת המדעי
Molecular Cell, חושפים את עקרונות הפעולה של "קוד הבקרה" של הגנום: מתברר, שגורמי הבקרה פועלים באופן היררכי, כשהם מחולקים לשלוש דרגות. החוקרים מיפו את פעילותם של 50 גורמי בקרה, בנקודות זמן שונות, בתאי חיסון שנחשפו לנגיף, וכך, למעשה, הצליחו לרדת לפרטי הפרטים של המנגנונים המווסתים תגובה חיסונית מסוג זה.
"בימים אלה מתקיים מירוץ דומה בחשיבותו ובמורכבותו למיפוי גנום האדם - המאמץ להבין את השינויים הגנטיים באזורי הבקרה, ואת הקשר שלהם למחלות ולשונות בין בני אדם", אומר ד"ר עמית. "המירוץ הזה נתקל במכשול משמעותי: התהליך שאמצעותו ממפים מנגנוני בקרה כבר 30 שנה הוא מורכב, מסובך ואיטי, משום שהוא נעשה באופן ידני, דוגמה אחר דוגמה. לכן נעשו מחקרים כאלה רק על-ידי צוותי-ענק של מדענים. באמצעות השיטה החדשה הצלחנו – קומץ אנשים – לבצע מחקר בקנה- מידה זהה, אך בחלקיק הזמן". המטרה היא לזהות את החלבונים הנקשרים לרצפי הבקרה (הקרויים "גורמי שיעתוק"), ולקבוע איזה חלבון נקשר לאיזה רצף, באיזה תא, ובאיזה מצב. לשם כך מקובעים החלבונים לדי-אן-אי, ולאחר מכן הדי-אן-אי עובר פיענוח ("ריצוף") לצורך קביעת המיקום המדויק שבו נקשר החלבון לגנום. השיטה שפיתח ד"ר עמית משלבת אוטומציה מתקדמת ושיטות חישוביות, ומודדת במקביל כמות גדולה של חלבונים.
המדענים חשפו תאים מסוימים של המערכת החיסונית לחיידקים, ולאחר מכן עקבו אחר 50 חלבוני בקרה הידועים כחשובים לתגובה החיסונית, בארבע נקודות זמן שונות. כך עלה בידיהם לזהות את אתרי הקישור אליהם נקשרים חלבוני הבקרה, לקבוע אילו גנים הם מפעילים, באיזו רמה, ובאילו מנגנונים. בנוסף, הם גילו כי קיימת היררכיה בפעילותם של 50 החלבונים, וכי ניתן לסווג אותם לאחת משלוש רמות: הרמה הראשונה של גורמי בקרה היא הקובעת את זהותו הבסיסית של התא ואת מסלול ההתמיינות שלו. גורמים אלה מסוגלים לבדם לקבוע את תכונות התאים המרכיבים את רקמות השריר, את אלה היוצרים את מערכת העצבים, וכדומה. בעוד הרמה הראשונה של גורמי הבקרה יוצרת חלוקה גסה לזהויות בסיסיות של תאים, הרמה השנייה קובעת תת-זהויות, באמצעות ויסות עוצמת הביטוי של הגנים. כך נוצרים, לדוגמה, ההבדלים בין תאים שונים של מערכת החיסון, או בין תאי שריר חלק לבין תאי שריר משורטט. הרמה השלישית של הבקרה היא הספציפית ביותר, ומשפיעה על ביטויים של גנים מסוימים. ברמה זו נקבעת תגובת התאים לגורמים חיצוניים: פלישת חיידקים, איתות הורמונלי, רעב ועוד.
הבנת המבנה ההיררכי מאפשרת לחזות כיצד יתבטאו מחלות הנגרמות עקב פגמים בגורמי הבקרה. שיבושים בגורמי בקרה מהרמה השלישית עלולים לפגוע, לדוגמה, ביכולתו של הגוף להתמודד עם מחלות נגיפיות. שיבושים בגורמי הבקרה מהרמה הראשונה עשויים לגרום לוקמיה, משום שבמחלה זאת נפגעים מסלולי ההתמיינות של תאי הדם. בנוסף, בהבנה מעמיקה של תוכנית הבקרה טמון גם פוטנציאל בתחום הרפואה השיקומית, שכן היא מאפשרת לגרום להתמיינות מחודשת של תאים באמצעות גורמי הבקרה המתאימים. חולים הזקוקיםלהשתלת תאים מסוג מסוים יוכלו להשתמש בתאים שלהם-עצמם לאחר שימוינו מחדש, וכך להתגבר על הקושי שבמציאת תורם מתאים.
ד"ר עמית: "השיטה החדשה למיפוי תוכנית הבקרה הגנטית פותחת אפיקים חדשים למדידת תהליכים ביולוגיים ולהבנה עמוקה שלהם, וכך תסייע להבין את השיבושים המתרחשים במחלות שונות. דוגמה לכך היא מחלת הלוקמיה, אשר קשורה בגורמי בקרה כאלה. תהליכי מחלה זו נחקרים על-ידי בימים אלה, בשיתוף עם פרופ' שי יזרעאלי מהמרכז הרפואי בתל השומר".
עידו עמית גדל בקיבוץ יזרעאל, וכבר מילדותו הסתקרן לדעת כיצד פועלות מכונות ביולוגיות, וכיצד אפשר לתקן ולשפר אותן. הסקרנות הזו הובילה אותו ללמוד מדעי החיים: את התואר הראשון והשני עשה באוניברסיטת בר-אילן, ואת התואר השלישי במכון ויצמן למדע, בהדרכתו של פרופ' יוסף ירדן, במחלקה לבקרה ביולוגית. לאחר מכן יצא למחקר בתר-דוקטוריאלי במכון Broad של המכון הטכנולוגי של מסצ'וסטס (MIT) ושל אוניברסיטת הרווארד. בשנת 2011 הצטרף לסגל המחלקה לאימונולוגיה במכון ויצמן למדע, שם הוא חוקר את מערכת החיסון מזווית גנומית ומערכתית.
עידו עמית מתגורר במכון עם אשתו דנה ועם שלושת ילדיו: עומרי בן 13, יונתן בן 9, ועלמה בת שנה. בזמנו הפנוי הוא רוכב על אופני כביש ושטח.

