תאי לוקמיה מצליחים לעשות את מה שאנשים רבים חולמים לעשות. הם מצליחים לחיות כמעט לנצח. איך הם עושים זאת? מדעני מכון ויצמן למדע גילו, שבכרבע ממקרי הלוקמיה מופעל בתאים הסרטניים "מאזן אימה" פנימי האחראי להישרדותם ולהתרבותם. כאשר מתחוללת מוטציה בגרסה של גן מסוים, הופך הגן שבו התרחשה המוטציה לגן מקדם סרטן - אונקוגן. אולם, מתברר, דווקא הגרסה המקורית,
הנורמלית, של הגן, לצד גרסת המוטציה, היא שמחזיקה את התא הסרטני בחיים, שומרת על אופיו הסרטני, ומאפשרת לו לגרום נזק הרסני לגוף. ממצאים אלה
התפרסמו באחרונה בכתב-העת המדעי
Cell Reports.
הגן שבו מדובר, RUNX1, ממלא תפקיד חיוני בהתפתחות מערכת הדם ובתחזוקתה. הגן מקודד לחלבון המתפקד כגורם שיעתוק: חלבון השולט בהתבטאותם של גנים רבים אחרים. במערכת הדם מנחה RUNX1 את התמיינותם של תאי גזע המצויים בלשד העצם, כך שיתפתחו לסוגים שונים של תאי דם בוגרים. די במוטציה בודדת בגן RUNX1 בתאי גזע אלה כדי לדרדר אותם במדרון החלקלק המוביל להתמרה סרטנית. דוגמה לכך היא הלוקמיה המיילואידית החריפה (AML), שנגרמת בעקבות סוג מסוים של מוטציה המתרחשת כאשר חלק מכרומוזום 8 נודד אל תוך הגן RUNX1, בכרומוזום 21. כתוצאה מכך נוצר גן סרטני (אונקוגן) המבטא חלבון מאוחה, אשר כולל הן מרכיבים של RUNX1 והן מרכיבים שמקורם בפיסה הגנטית הנוספת. החלבון המאוחה הוא זה שגורם לוקמיה. בתהליך דומה מתפתחת הלוקמיה הנפוצה ביותר בקרב ילדים, ALL.
"החלבון הסרטני המאוחה, המווסת באופן ישיר את פעילותם של גנים רבים, גורם סדרה של שינויים גנטיים נוספים בתא", אומר
פרופ' יורם גרונר מהמחלקה לגנטיקה מולקולרית, שעמד בראש צוות המחקר, וביצע בעבר מספר מחקרים שהתמקדו בגן RUNX1 ובגנים נוספים המצויים על כרומוזום 21. במחקרים אלה הצליח פרופ' גרונר, בין היתר, לפענח את תפקידו של RUNX1 בלוקמיה התוקפת חולי תסמונת דאון.
את המחקר הנוכחי הוביל החוקר הבתר-דוקטוריאלי ד"ר אורן בן עמי, מקבוצתו של פרופ' גרונר, והשתתפו בו חברי קבוצת המחקר של ד"ר עמוס תנאי מהמחלקה למדעי המחשב ומתמטיקה שימושית, ודינה לשקוביץ מהמרכז הלאומי לרפואה מותאמת אישית, הפועל במכון ויצמן למדע. כהכנה למחקר הנוכחי סרקו המדענים מיגוון מאגרי מידע, והבחינו בתופעה יוצאת דופן: הנתונים הקליניים רמזו, כי העותק הנורמלי של הגן RUNX1 – זה שלא התרחשה בו מוטציה – נשמר תמיד בתאים הלוקמיים, ופעילותו גבוהה. ידוע, כי בכל אחד מתאי גופנו מצויים שני עותקים של כל גן: אחד שמקורו באם ושני שמקורו באב. המוטציות הגורמות סרטן מתרחשות רק באחד משני העותקים האלה, וגורמות את התפתחות המחלה. העותק הבריא, לעומתו, מושתק בדרך כלל, כך שרק העותק המוטנטי בא לידי ביטוי.
במקרה זה נראה, כי העותק הבריא של RUNX1 אינו מושתק בתאים הלוקמיים. עובדה זו העלתה את ההערכה, כי העותק הבריא ממלא גם הוא תפקיד בהתפתחות המחלה. אולם כיצד הוא עושה זאת, ובאיזה שלב?
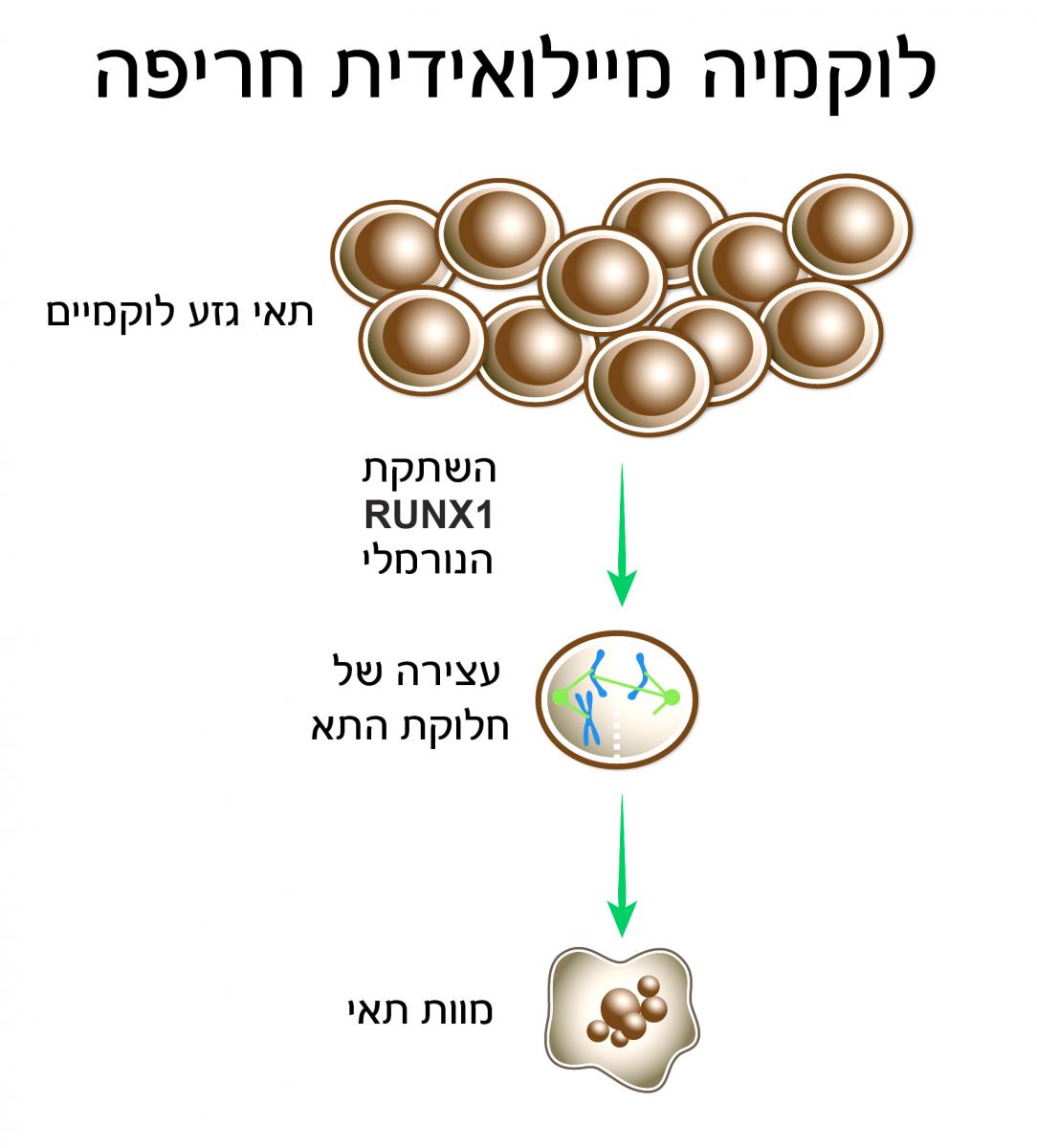
כדי לענות על שאלה זו גידלו המדענים תאים לוקמיים, שבחלקם הושתק העותק המוטנטי של הגן RUNX1, בחלקם הושתק העותק הנורמלי, ובחלקם פעלו שני העותקים כרגיל. התברר, שכאשר העותק הנורמלי מושתק, התאים מתים. לעומת זאת, התאים בהם היו שני העותקים פעילים שמרו על אופיים הסרטני. בדיקה מדוקדקת הראתה, כי תאים סרטניים אלה הצליחו לחמוק ממסלול של מוות תאי אשר קרוי אפופטוזיס – מנגנון התאבדות שנועד, בין היתר, למנוע את הישרדותם ואת התרבותם של תאים הנושאים מוטציות סרטניות. במילים אחרות, נראה כי העותק הנורמלי של RUNX1, ולא העותק המוטנטי, הוא האחראי להישרדותם העקשנית של התאים הסרטניים – אחת מתכונותיהם המסוכנות ביותר.
פרופ' גרונר אומר, שהתאים הלוקמיים "מכורים" לגרסה הנורמלית של RUNX1, כלומר, הם תלויים בה באופן פיסיולוגי לצורך הישרדותם. "במהלך הזמן רוכש הגן האונקוגני המאוחה 'מומחיות' בהפיכת התאים לתאים סרטניים. ככל שהתהליך הסרטני התוך-תאי מתקדם, התא זקוק ל'מאזן האימה' בין שתי הגרסאות של הגן כדי להתקיים".
התובנה החדשה מחוללת מהפכה בהבנת הלוקמיה. המדענים סבורים, כי התגלית המפתיעה תוביל לפיתוח שיטות מתקדמות, יעילות ומדויקות, לאיבחון סוגים אלה של לוקמיה, ולטיפול במחלה.