ללא קולגן היינו מתפרקים – במלוא מובן המלה. מולקולת החלבון הגדולה הזו, הנפוצה ביותר בגופנו, היא ה"דבק" המדביק את הרקמות. למעשה, בעבר האבולוציוני הרחוק שלנו היה זה הקולגן שאיפשר לאבותינו הקדמונים החד-תאיים להתפתח ליצורים רב-תאיים – משום שהוא סייע לתאים בודדים להיצמד זה לזה.
בזמן התפתחות העובר נוצרות בו כמויות גדולות של קולגן, חומר-המוצא לבניית העצם. מאחר שהפקת הקולגן היא תהליך מורכב ורב-שלבי, אשר דורש חמצן רב, ניתן היה לצפות כי העצם הצומחת תקבל אספקה גדולה של חמצן. אך באופן מפתיע, בדיוק ההיפך הוא הנכון. העצם, כאיבר פנימי, מקבלת כמויות קטנות של חמצן – ביחס לרקמות החיצוניות של העובר. יתר על כן, רקמת הסחוס, המקדימה את היווצרות העצם, דוחה מתוכה החוצה באופן פעיל את כלי הדם הנושאים את החמצן.
.jpg)
מחקר שנעשה במכון ויצמן למדע ופורסם בכתב-העת
Development שופך אור חדש על הפרדוקס. אמנם, החידה הנוגעת להיווצרות העצם בנוכחות חמצן מועט כל כך טרם נפתרה, אך ממצאי המחקר מסבירים כיצד בכל זאת מיוצר הקולגן בתנאים שהם לכאורה כל כך לא מתאימים.
.jpg) פרופ' אלעזר זלצר, ליטל בן טובים, ותלמיד המחקר דאז ד"ר רועי אמריגליו, מהמחלקה לגנטיקה מולקולרית, חקרו את היווצרות הקולגן בעצם הצומחת של עוברי עכבר. הם התמקדו במולקולה הקרויה HIF1-α, אשר ממלאת תפקיד מרכזי בבקרת תגובת התא לרמות חמצן נמוכות ברקמות. המדענים גילו, כי HIF1-α מתפקדת גם כמתג בקרה מרכזי בבניית הקולגן, והופכת את התהליך ליעיל ביותר, על מנת לנצל את מעט החמצן באופן מיטבי. כאשר חסמו המדענים את פעילותה של מולקולה זו, נפגע ייצור הקולגן, והעצם לא צמחה כראוי.
פרופ' אלעזר זלצר, ליטל בן טובים, ותלמיד המחקר דאז ד"ר רועי אמריגליו, מהמחלקה לגנטיקה מולקולרית, חקרו את היווצרות הקולגן בעצם הצומחת של עוברי עכבר. הם התמקדו במולקולה הקרויה HIF1-α, אשר ממלאת תפקיד מרכזי בבקרת תגובת התא לרמות חמצן נמוכות ברקמות. המדענים גילו, כי HIF1-α מתפקדת גם כמתג בקרה מרכזי בבניית הקולגן, והופכת את התהליך ליעיל ביותר, על מנת לנצל את מעט החמצן באופן מיטבי. כאשר חסמו המדענים את פעילותה של מולקולה זו, נפגע ייצור הקולגן, והעצם לא צמחה כראוי.
המדענים מצאו, כי HIF1-α פועל כמו מנהל מוכשר: הוא מייצר תנאים מיטביים לבניית הקולגן. ראשית, הוא מגביר את יצירת האנזימים הקטליטיים המזרזים את התהליך. בנוסף, הוא עוצר תהליכים אחרים של חילוף החומרים ברקמה, כדי שמעט החמצן הקיים יופנה כולו לתאים המייצרים את הקולגן, במטרה לאפשר להם להתרכז במשימה זו בלבד.
ממצאים אלה מבהירים כיצד נוצרות אבני בניין מהמרכזיות ביותר בגוף העובר. בנוסף, המחקר עשוי לתרום להבנת מחלות. לדוגמה, הוא עשוי להציע הסבר לשאלה, מדוע רמות נמוכות של חמצן ברקמות סרטניות אינן מונעות את התפתחות הגידול.
מחוברים
עצמות, שרירים וגידים מקנים לגופנו את צורתו, שומרים על יציבותו, ומאפשרים לו לנוע. אך כדי לבצע תפקידים אלה באופן מוצלח עליהם להוות מערכת אחת בעלת חלקים מתואמים בדיוק רב – מערכת השלד והשרירים.
מחקר חדש שנעשה במכון ויצמן למדע ופורסם בכתב העת
Development גילה מנגנון מרכזי האחראי ליצירת המערכת.
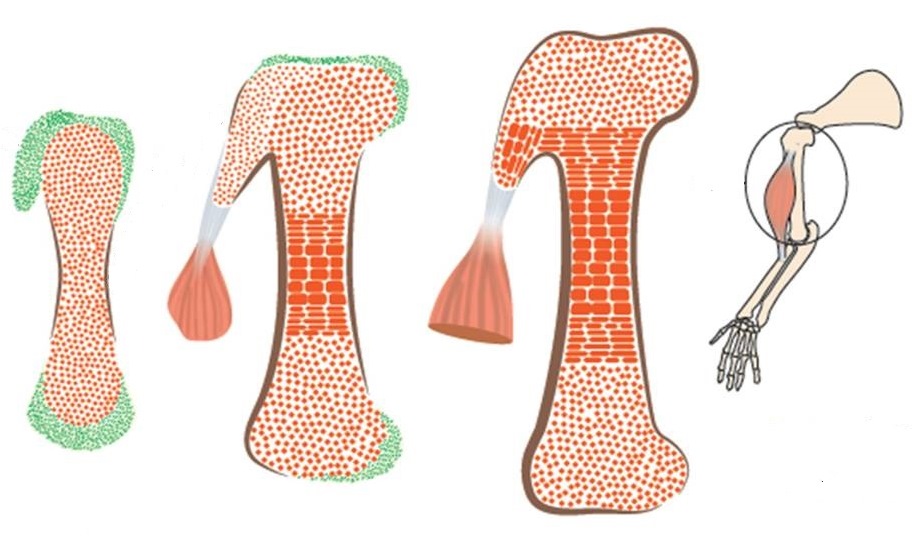
שלב בסיסי בהרכבת מערכת השלד והשרירים הוא התפתחות יחידות החיבור בין העצם לבין הגידים. אלה הן בליטות בעלות צורות וגדלים שונים, הצומחות על פני השטח של העצם. בליטות אלה חיוניות לתיפקודה התקין של מערכת השלד והשרירים: הן מהוות נקודות אחיזה יציבות עבור השרירים, הנצמדים לעצם באמצעות הגידים, ומפזרות את המתח שמפעילים השרירים המתכווצים על העצם.
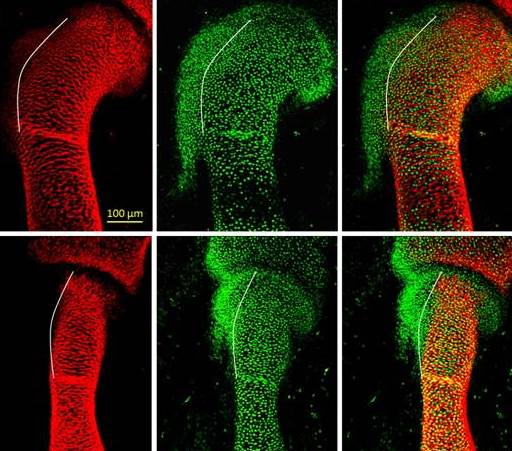
במחקר החדש, אשר נעשה בעוברי עכבר, גילו המדענים כי בליטות העצם נוצרות מקבוצת תאים שונה מהתאים בוני-העצם המוכרים, אשר לא הייתה ידועה קודם לכן. התאים בוני-הבליטות מתאפיינים במעין "פיצול אישיות": הם נשלטים בעת ובעונה אחת על-ידי שתי תוכנות גנטיות – אחת המתאימה לעצם, ושנייה המתאימה לגידים. הפיצול הזה הוא המאפשר את התחברותם של הגידים והשרירים אל
בליטות העצם.
המדענים פיענחו את פרטי שתי התוכנות הגנטיות, ובכלל זה את מנגנוני הבקרה המולקולריים שלהן, באמצעות יצירת עוברי עכברים מוטנטים, בהם חסרו גנים מסוימים, ומעקב אחר התפתחותם. את המחקר ביצעו פרופ' אלעזר זלצר ותלמידת המחקר דאז ד"ר עינת בליץ, מהמחלקה לגנטיקה מולקולרית במכון.
הגילוי שהעצמות נוצרות בעובר באופן מודולרי עשוי לעזור להסביר את התכונות המכניות שלהם, למשל, את יכולתם של אזורים אנטומיים שונים של העצם להתמודד בדרכים שונות עם מתח ועם משקל, דבר התורם לעמידתו ולגמישותו של השלד.

.jpg)
.jpg) פרופ' אלעזר זלצר, ליטל בן טובים, ותלמיד המחקר דאז ד"ר רועי אמריגליו, מהמחלקה לגנטיקה מולקולרית, חקרו את היווצרות הקולגן בעצם הצומחת של עוברי עכבר. הם התמקדו במולקולה הקרויה HIF1-α, אשר ממלאת תפקיד מרכזי בבקרת תגובת התא לרמות חמצן נמוכות ברקמות. המדענים גילו, כי HIF1-α מתפקדת גם כמתג בקרה מרכזי בבניית הקולגן, והופכת את התהליך ליעיל ביותר, על מנת לנצל את מעט החמצן באופן מיטבי. כאשר חסמו המדענים את פעילותה של מולקולה זו, נפגע ייצור הקולגן, והעצם לא צמחה כראוי.
פרופ' אלעזר זלצר, ליטל בן טובים, ותלמיד המחקר דאז ד"ר רועי אמריגליו, מהמחלקה לגנטיקה מולקולרית, חקרו את היווצרות הקולגן בעצם הצומחת של עוברי עכבר. הם התמקדו במולקולה הקרויה HIF1-α, אשר ממלאת תפקיד מרכזי בבקרת תגובת התא לרמות חמצן נמוכות ברקמות. המדענים גילו, כי HIF1-α מתפקדת גם כמתג בקרה מרכזי בבניית הקולגן, והופכת את התהליך ליעיל ביותר, על מנת לנצל את מעט החמצן באופן מיטבי. כאשר חסמו המדענים את פעילותה של מולקולה זו, נפגע ייצור הקולגן, והעצם לא צמחה כראוי.