עיתונאיות ועיתונאים, הירשמו כאן להודעות לעיתונות שלנו
הירשמו לניוזלטר החודשי שלנו:
מדעני המכון גילו מנגנון חדש של "האצה ובלימה", אשר שולט בקצב אובדן הסיבים העצביים ובגיזומם בשלבי ההתפתחות העוברית. ייתכן שמחלות ניוון עצבי פועלות באמצעות 'חטיפה' של רכיבים מסוימים במערכת העצבים טרם הבשלתה.

כולנו מרוטי-עצבים, במלוא מובן המלה. תאי העצב שלנו, בדומה לעצים, שולחים ענפים דקים וארוכים, הקרויים אקסונים, אשר נושאים אותות אל כל חלקי הגוף. בהתפתחות עוברית תקינה, נוצר עודף ניכר של אקסונים. ברובם יתרחש "גיזום" טבעי – תהליך שנועד להבטיח שייוותרו בגוף רק חיבורים חיוניים, וזאת לצורך פעילותה התקינה של מערכת העצבים.
לאחר הבשלת מערכת העצבים, אובדן של אקסון או תא עצב מתרחש בדרך כלל במקרים של פציעה חמורה או מחלת ניוון עצבי דוגמת טרשת אמיוטרופית צידית (Amyotrophic lateral sclerosis – ALS), ונוירופתיה פריפרית (Peripheral Neuropathy). תהליכי ההתפתחות של מחלות אלה אינם מובנים לנו די הצורך, דבר שכמובן מקשה על פיתוח של תרופות ושיטות טיפול יעילות.
פרופ' אברהם ירון, ותלמידת המחקר לשעבר מאיה מאור-נוף, מהמחלקה למדעים ביומולקולריים במכון ויצמן למדע, מאמינים שהבנת המנגנונים אשר מעצבים את מערכת העצבים במהלך ההתפתחות העוברית, ובשנות החיים הראשונות, עשויה להעלות תובנות גם ביחס למחלות של ניוון עצבי. במחקרם, שפורסם באחרונה בכתב-העת המדעי Neuron, גילו המדענים מנגנון חדש של "האצה ובלימה" אשר שולט בקצב אובדן האקסונים ובגיזומם בשלבי ההתפתחות, וזיהו בו פעילות של גנים המעורבים במודלים של פגיעה עצבית אשר משמשים נושא למחקר.
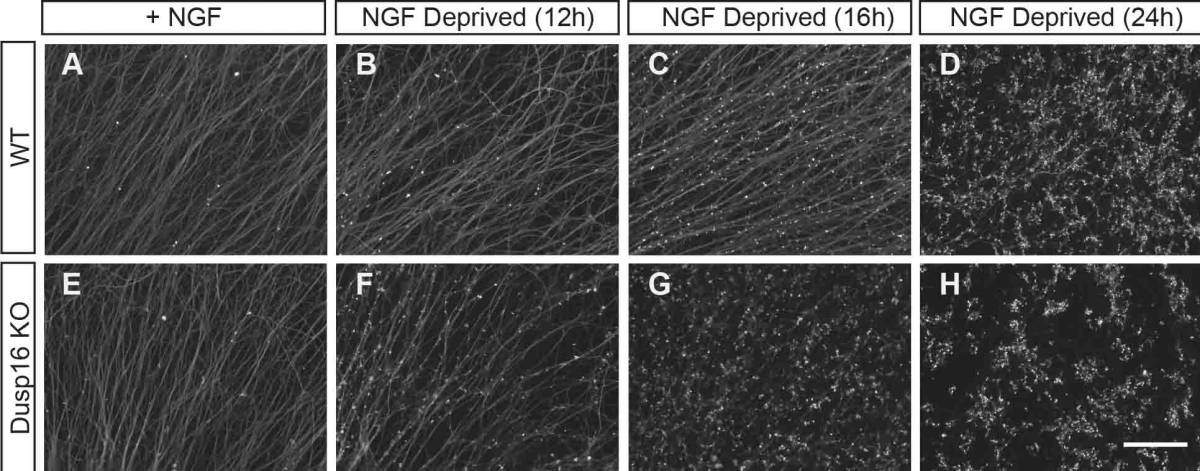
המדענים גידלו תאי עצב חושיים על מצע שהכיל גורמי גידול – ואז, כדי לדמות תהליך גיזום התפתחותי – הרחיקו את גורמי הגידול מהמצע, ובדקו אילו גנים הגיבו לכך בהתבטאות מוגברת. את רשימת הגנים שבידיהם הישוו לקבוצות גנים אחרות, אשר מתבטאים בתגובה לפגיעה עצבית. גן אחד כזה – Dusp16 – הופיע באופן בולט בשתי הקבוצות, ולכן החליטו המדענים לחקור אותו לעומק, כדי לבדוק אם יש לו תפקיד בתהליכי פירוק.
באופן מפתיע מצאו החוקרים, שדווקא בנוירונים שחסרו את הגן והחלבון שאותו הוא מקודד, התפרקו האקסונים מהר יותר. מכאן הסיקו, שהחלבון Dusp16 הוא מעכב או "בלם", אשר מאט את תהליך הפירוק, ואינו מעודד פירוק, כפי שסברו.
כדי להבין את פעילות החלבון, שבו המדענים אל השוואת רשימות הגנים אשר ביטויָים הוגבר בתגובה לגיזום התפתחותי או לפגיעה עצבית, ומצאו גן משותף נוסף לשתי הקבוצות - Puma. בעבר הוכח שתוצרו של גן זה, החלבון Puma, הוא חלק מהמערכת של מוות תאי "מתוכנת", אשר נועד לגרום להתאבדות תאים, כדי להימנע מגרימת נזק לאורגניזם השלם. האם עובדה זו קשורה לפעילות החלבון Dusp16? כדי לענות על שאלה זו, בחנו המדענים תאי עצב חסרי Dusp16. כך הם גילו, שבהיעדרו מתגבר ביטויו של החלבון Puma. ממצא זה מחזק את הסברה, שלגן Dusp16 יש תפקיד הגנתי. בהמשך התגלה גם, שבתאי עצב חסרי Dusp16 נעשה החלבון p53 – חלבון חיוני לביטוי החלבון Puma – "היפראקטיבי". בשלב זה הצליחו החוקרים לחבר את שרשרת האירועים המתרחשים בתנאים רגילים. לפי ממצאיהם, בתגובה להרחקת גורמי הגידול מהמצע משהה Dusp16 את p53, אשר נחוץ לביטויו של הגן Puma, ובכך הוא מעכב פירוק או גיזום של אקסונים.
"הופתענו לגלות, שבמקום שתהליך הגיזום ינוע ב'תאוצה מלאה' קדימה לאחר שיצא לדרך, תא העצב משתמש בתוכנית פעילה – בדמות Dusp16 – כדי למנוע או להאט את תהליך הפירוק", אומר פרופ' ירון. "הממצאים שלנו מצביעים על האפשרות, שמחלות ניוון עצבי פועלות באמצעות 'חטיפה' של רכיבים מסוימים בתהליך ההתפתחותי במערכת העצבים, טרם הבשלתה; למשל, הן עשויות לגרום לאובדן של מעכבים כמו Dusp16, או לביטוי-יתר של גנים מעודדי-פירוק דוגמת Puma – ובכך, להאיץ ניוון תאי עצב".
בסקירה שפורסמה באחרונה בכת העת Current Biology מסבירים פרופ' ירון ופרופ' אורן שולדינר, מהמחלקה לביולוגיה מולקולרית של התא, כי גילוי קווי דמיון בין גיזום עצבי בהתפתחות תקינה לבין ניוון במצבי מחלה עשוי לסלול את הדרך לפיתוח דרכי טיפול לריפוי מחלות אלו או להאטת קצב החרפתן.
כ-50% מהנוירונים מתים תוך כדי הבשלת מערכת העצבים במהלך ההתפתחות העוברית, ואף לאחר הלידה. #מספרי_מדע |