עיתונאיות ועיתונאים, הירשמו כאן להודעות לעיתונות שלנו
הירשמו לניוזלטר החודשי שלנו:
מחלת השחפת היא עדיין מגורמי המוות המרכזיים בעולם. עלייתם של זני שחפת עמידים לאנטיביוטיקה מחייבת גישות טיפול חדשות. מעטה עבה דמוי שעווה מאפשר לחיידק מחולל המחלה להסתתר מפני מערכת החיסון, ואף למנוע חדירה של תרופות אנטיביוטיות. מדעני מכון ויצמן למדע הפנו מבט אל המערכת שמייצרת את "מעטה הסתרים" של החיידק באמצעות שיטה חדשנית של מיקרוסקופיה אלקטרונית, ומיפו את המבנה שלה ברמת דיוק חסרת תקדים. ממצאי המחקר, שפורסמו באחרונה בכתב-העת המדעי Nature Communications, עשויים לסלול את הדרך לגישות טיפול חדשות שיאפשרו להתגבר על העמידות לאנטיביוטיקה.
ברוב התאים החיים קיימת אחת משתי מערכות סינתזה של חומצות שומן (FAS), שהן מכלולים המורכבים מכמה אנזימים. מערכות אלו מייצרות מולקולות מבוססות שומן המרכיבות את קרומי התא. בבעלי-חיים ובפטריות יש בדרך כלל מערכת מסוג 1 (FAS-I), בחיידקים ובחיידקים קדומים (Archaea) – מערכת מסוג 2 (FAS-II). "חיידק השחפת מכיל את שתי המערכות, אשר משתפות פעולה בייצור חומצות שומן ארוכות במיוחד – עד 90 קשרי פחמן בשרשרת, לעומת חומצות שומן עם 16 פחמנים בתאי אדם", מסביר ד"ר רון דיסקין מהמחלקה לביולוגיה מבנית. לאורך עשור של מחקר, אסף פרופ' אורן צמחוני מהמרכז הרפואי קפלן, המסונף לבית הספר לרפואה של האוניברסיטה העברית בירושלים, ראיות לכך שמערכת FAS-I בחיידק השחפת עשויה להיות יעד מצוין למתקפה תרופתית. עם זאת, גודלם הרב של מכלולי FAS-I הופך אותם למאתגרים במיוחד למיפוי ולמחקר.

האתגר הראשוני היה לבודד את מכלול FAS-I מחיידק השחפת. לשם כך פנה פרופ' צמחוני למדעני המכון – פרופ' ציפורה שקד מהמחלקה לביולוגיה מבנית ופרופ' יגאל בורשטיין מהמחלקה לכימיה אורגנית. במאמר שהתפרסם בכתב-העת המדעי PLoS One, תיאר פרופ' צמחוני את השיטה לבידוד FAS-I מהחיידק שפיתח צוות המחקר שכלל את הביוכימאי המוכשר, אלון שוורץ המנוח, וד"ר משה פרץ מהמחלקה לביולוגיה מבנית. למרות פריצת הדרך, החוקרים לא הצליחו להפיק גבישי FAS-I באיכות הנדרשת לניתוח מבני באמצעות קריסטלוגרפיה בקרני רנטגן. אף על פי כן, ניתוח ראשוני במיקרוסקופיית אלקטרונים (EM) הצביע על פוטנציאל משמעותי לשיטה זו כדרך לניתוח מבני של FAS-I.
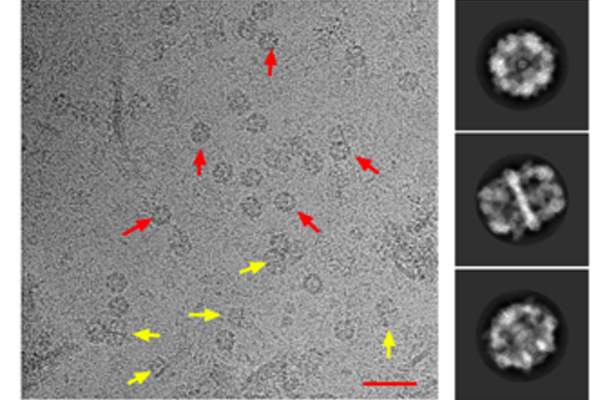
בשלב זה, פנו פרופ' צמחוני ופרופ' שקד לד"ר דיסקין, והשלושה החליטו לאמץ גישה חדשנית של מיקרוסקופיית אלקטרונים קריוגנית של חלקיקים בודדים (single particle cryo-EM). בעזרת ד"ר נדב אלעד מהמחלקה לתשתיות מחקר כימי וחוקרים נוספים, הוכנו רשתות פחמן דקיקות המכילות מולקולות FAS-I שהועברו למיקרוסקופ אלקטרונים מיוחד בהיידלברג שבגרמניה. בשלב הבא, נעזר צוות המחקר באלגוריתמים לתרגום הנתונים מהיידלברג לתמונות תלת-ממדיות שחשפו את מבנה FAS-I ברמת האטום כמעט. החוקרים השוו את המבנה שקיבלו עם המבנה של מערכת FAS-I בפטריות, ומצאו יותר הבדלים ממה שציפו, בייחוד באזורים שבהם מיוצרות השרשרות של חומצות השומן. הבדלים אלה הם ככל הנראה הסיבה לכך שמערכתFAS-I בחיידק מתאימה לייצור שרשרות ארוכות יותר.
הגענו לרזולוציה הנדרשת כדי להתחיל לתכנן תרופה, שכן אנו רואים כעת לא רק צורה כללית, אלא גם היכן וכיצד מולקולה של תרופה יכולה להיקשר ולעכב את פעולת האנזים"
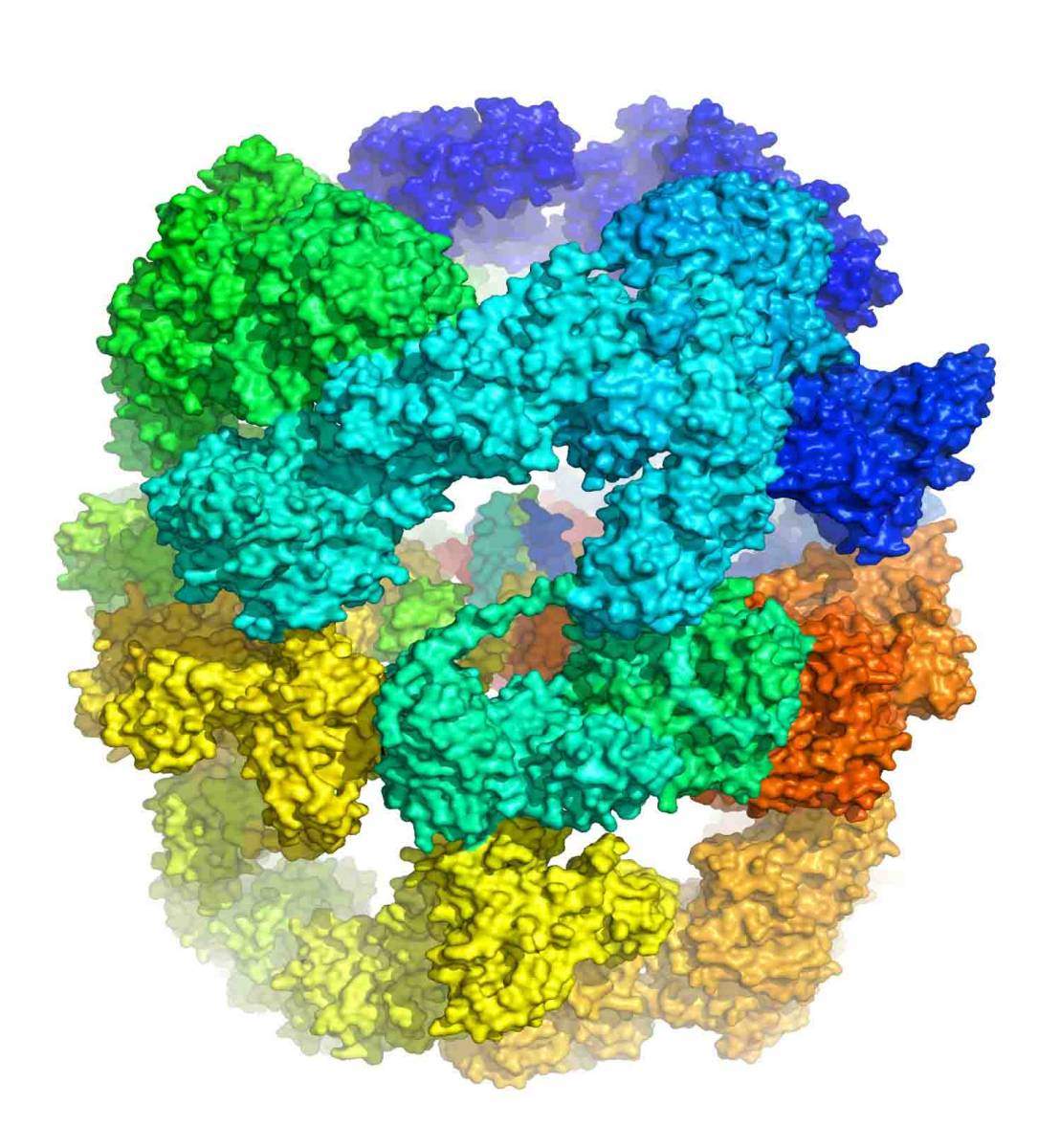
"הגענו לרזולוציה הנדרשת כדי להתחיל לתכנן תרופה, שכן אנו רואים כעת לא רק צורה כללית, אלא גם היכן וכיצד מולקולה של תרופה יכולה להיקשר ולעכב את פעולת האנזים", אומר ד"ר דיסקין. "למעשה, קיימת כבר כיום גרסה אחת של תרופה כזו – Pyrazinamide (או בקיצור PZA) שמקצרת את זמן הטיפול בחולי שחפת מעד שנה לכמה חודשים". פרופ' צמחוני ועמיתיו הראו כי PZA ומולקולות דומות עשויות לעכב את מכלול FAS-I. כעת, כאשר מבנה המכלול ידוע, אפשר יהיה להעמיד את התיאוריה למבחן, וכן לבחון מולקולות חדשות. באופן מיטבי, תרופות אלו יפעלו ביחד עם אנטיביוטיקה ויחשפו את האזורים הפנימיים של החיידק לפעולת מערכת החיסון. ד"ר דיסקין מוסיף: "פרויקט זה מדגים היטב איך, למרות מכשולים ניסויים רבים, אפשר למפות יעדים מאתגרים במיוחד".
במחקר השתתפו גם ד"ר סילביה ברון וגל רביב מהמחלקה לביולוגיה מבנית; ד"ר דוד מורגנשטרן וד"ר ישי לוין מהמכון למיפוי חלבונים על-שם דה בוטון במרכז הישראלי הלאומי לרפואה מותאמת אישית על-שם ננסי וסטיבן גרנד; ד"ר שרון וולף, ראש יחידת מיקרוסקופיית האלקטרונים במחלקה לתשתיות מחקר כימי; וד"ר יואב פלג, ד"ר שירה אלבק, ד"ר יעקב גרינולד וד"ר אורלי דים מהיחידה לפרוטאומיקה מבנית.
1.6 מיליון בני-אדם בעולם מתו משחפת ב-2017, וכ-10 מיליון חולים חדשים נדבקו במחלה, לפי נתוני ארגון הבריאות העולמי. #מספרי_מדע |