עיתונאיות ועיתונאים, הירשמו כאן להודעות לעיתונות שלנו
הירשמו לניוזלטר החודשי שלנו:
מחלות ממאירות מתפתחות כאשר תאים מאבדים שליטה ומתרבים ללא בקרה. מאמצי המחקר בעולם מכוונים לפיענוח "תוכנית האב" של תאים סרטניים – ולהבנה כיצד הם משתלטים על מסלולי גדילה המסייעים להם להתרבות ולהתפשט באופן לא מבוקר. הבנת מנגנונים אלה עשויה לסייע בפיתוח דרכים יעילות להילחם במחלה.
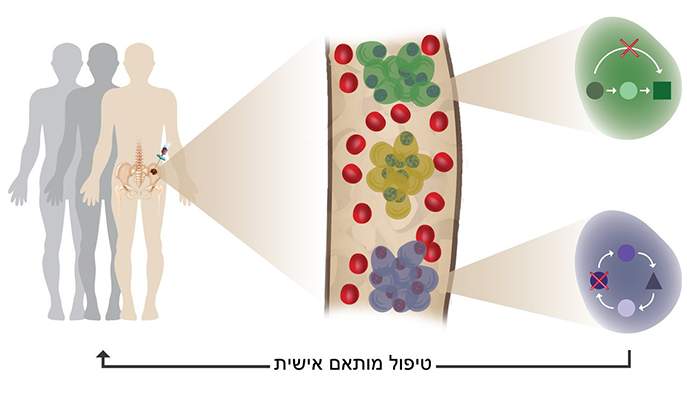
שיתוף פעולה בין מדענים ממכון ויצמן למדע ורופאים מהמחלקות ההמטו-אונקולוגיות בישראל, הוביל לזיהוי מדויק של הפרופילים הגנטיים ה״אישיים״ של תאי סרטן דם מסוג מיאלומה נפוצה (Multiple Myeloma). במסגרת המחקר המשותף, זוהו פרופילים גנטיים של תאי הסרטן בארבע קבוצות חולים: חולים שהיו בשלב טרום-סרטני, חולי מיאלומה, חולים לאחר טיפול – וחולים שטופלו, הגיבו לטיפול, אך מחלתם חזרה והפכה לפעילה (relapse). המדענים והרופאים מעריכים שהמיפוי הגנטי האישי יסייע בעתיד בפיתוח שיטות חדשות לאבחון ולטיפול ממוקד במחלה קשה זו במסגרת ״רפואה מותאמת אישית״.
מיאלומה נפוצה היא סרטן הדם השני בשכיחותו. היא מתפתחת כאשר תאי פלסמה – התאים המייצרים נוגדנים בלשד העצם – מתרבים ללא שליטה ומובילים לכשל מערכות ולמוות. המחלה נחקרת שנים רבות, ובשנים האחרונות אף הושג שיפור משמעותי בהישרדות של החולים בה – באמצעות טיפולים אימונותרפיים; אך ברוב החולים המחלה חוזרת (relapse). אחד המכשולים המרכזיים בטיפול במיאלומה היא השונות הרבה בין החולים במחלה והקושי לאבחן את החולים בשלבים המוקדמים שלה ולהתאים להם את הטיפול האופטימלי.
תאי הפלסמה של קבוצת הביקורת היו דומים מאוד אלה לאלה, והציגו פרופיל גנטי אחיד ותקין של תאי פלסמה נורמליים. השוואת הדפוס הנורמלי לדפוסים שזוהו בחולים, הראתה שלכל חולה דפוס גנטי ייחודי"
לדוגמה, חולים המזוהים באקראי בבדיקת דם שגרתית כחולים בשלב הטרום-סרטני של המחלה, נשארים במעקב רפואי ללא טיפול (watch and wait). כל שנה כ-1% מהם מפתח את המחלה, אך עד למחקר הנוכחי, לא הייתה דרך להבדיל בין אלה שיפתחו מיאלומה, לבין אלה שלא יפתחו את המחלה.
ד"ר גיא לדרגור, רופא וחוקר, וד"ר אסף ויינר מקבוצת המחקר של פרופ' עידו עמית במחלקה לאימונולוגיה במכון ויצמן למדע, ביחד עם קבוצת המחקר של פרופ' עמוס תנאי מהמחלקה למדעי המחשב ומתמטיקה שימושית במכון ויצמן למדע, סברו כי ריצוף אר-אן-אי בתא בודד (single-cell RNA sequencing) – שיטה בעלת רגישות גבוהה ביותר שחברי הקבוצה פיתחו – עשוי לאפשר גישה חדשה להבנת הגורמים להתפרצות מיאלומה נפוצה וכן לאבחון ולטיפול במחלה.
המערך לשיתוף פעולה מדעי-קליני במכון ויצמן למדע, בראשות פרופ' גבי ברבש, סייע בגיוס כל מחלקות ההמטו-אונקולוגיה בישראל לשיתוף פעולה עם מדעני המכון במחקר הייחודי הזה.
שיטת המחקר החדשה מאפשרת לחוקרים לרצף אר-אן-אי באלפי תאים בודדים מדם החולה, או מלשד העצם שלו, וכך לקבל את הפרופיל הגנטי של אר-אן-אי בכל תא בנפרד. באמצעות ריצוף עשרות אלפי תאים מאנשים בריאים שעברו ניתוחי החלפת מפרק ירך, תיעדו המדענים בתחילה את "הפרופיל התקין" של תאי פלסמה נורמליים; קבוצת הבריאים היוותה את קבוצת הביקורת. תאי הפלסמה של קבוצת הביקורת היו דומים מאוד אלה לאלה, והציגו פרופיל גנטי אחיד ותקין של תאי פלסמה נורמליים. השוואת הדפוס הנורמלי לדפוסים שזוהו בחולים, הראתה שלכל חולה דפוס גנטי ייחודי – בחלק מהמטופלים אף נצפו כמה "שבטים" (Clones) של תאים עם פרופילים גנטיים שונים באותו החולה.
בשיטה הייחודית שפותחה במחקר, אפשר לזהות גם בדם, אפילו מספר קטן ביותר של תאים ממאירים, וזאת, גם בשלב מחלה מוקדם מאוד, טרום-סרטני. זיהוי תאים בבדיקת דם יוכל להחליף את ביופסיית לשד העצם הפולשנית (והכואבת) לצורך מעקב אחר החולים האלה. בדיקת דם פשוטה תאפשר זיהוי מוקדם, אבחנה מדויקת והחלטות מושכלות יותר באשר לטיפול, בהתבסס על פרופיל המחלה ה"אישי" של כל חולה.
המחקר והאנליזה הגנטית הרגישה והייחודית, שיושמה במחקר זה לראשונה בעולם, מתפרסמים היום בכתב-העת המדעי Nature Medicine, ויסייעו בקידום הרפואה הישראלית בחזית הטיפול בחולי מיאלומה.
זיהוי התאים הסרטניים הנדירים ואפיונם התאפשר באמצעות שיטות של בינה מלאכותית וביג דאטה, וזה הכיוון שהרפואה העתידית תצעד בו יותר ויותר"
פרופ' ברבש מציין שההישג הנוכחי הוא רק ההתחלה ביישום טכנולוגיות ריצוף אר-אן-אי בתאים בודדים במחקרים קליניים-גנומיים. "אנו מעורבים כעת בפיתוח שיתופי פעולה דומים בין חוקרים בבתי-חולים לבין מדעני מכון ויצמן למדע, במטרה לקדם הבנת מנגנונים, אבחון וטיפול במחלות נוספות: מסרטן ומחלות אוטואימוניות ועד לאלצהיימר".
"ניתוח גנומי בתא בודד היה מוגבל עד כה למספר מצומצם של מעבדות מחקר", אומר פרופ' עמית. "אנחנו מרחיבים את גבולות הטכנולוגיה כל העת, כך שתוכל בעתיד להפוך לכלי קליני חשוב לאבחון ולניטור מחלות ממאירות רבות בשלב הטרום-סרטני, או לניטור התפרצותן מחדש לאחר טיפול אונקולוגי. טכנולוגיה זו גם תתרום לפיתוח טיפולים אימונותרפיים חדשים ויעילים יותר, על בסיס מסד הנתונים העצום שנבנה על המחלה".
"זיהוי התאים הסרטניים הנדירים ואפיונם התאפשר באמצעות שיטות של בינה מלאכותית וביג דאטה (נתוני עתק), וזה הכיוון שהרפואה העתידית תצעד בו יותר ויותר", אומר ד"ר אסף וינר.
"בעתיד", אומר ד"ר לדרגור, "רופאים יוכלו לעקוב אחר המחלה בזמן אמת ולטפל בכל חולה בהתאם לפרופיל מחלתו האישי, אולי אף לפני הופעת הסימנים הראשונים".
לקבלת מידע נוסף, תמונות ולתיאום ראיונות:
משרד הדובר - מכון ויצמן למדע
08-9343856 news@weizmann.ac.il