הילכו שניים יחדיו בלתי אם נועדו? בפראפראזה על השאלה התנ"כית הרטורית הזאת אפשר לשאול: האם שניים שמגיעים לאותה מטרה יכולים להשיג תוצאות שונות? ככל שהדברים נוגעים לאינטרפרונים אלפא וביתא, נראה שהתשובה המפתיעה על השאלה הזאת היא: כן. זה בדיוק מה שקורה.
שני האחים, אינטרפרון אלפא ואינטרפרון ביתא, הם חלבונים הפועלים בקו ההגנה הראשון של המערכת החיסונית. שניהם נקשרים לאותם קולטנים המוצגים על קרומי התאים, ושניהם מפעילים אותן מערכות תקשורת תוך-תאיות. אבל, בדרך מיסתורית כלשהי, נראה ששתי הפעולות האלה לא תמיד מובילות לאותן תוצאות, כך שלעתים הן מפעילות גנים שונים, בעוצמות שונות.
כיצד מתבצעת ההבחנה בין שתי הפעולות הזהות? תעלומה זו מעסיקה את ד"ר גדעון שרייבר מהמחלקה לכימיה ביולוגית במכון ויצמן למדע. פתרון התעלומה, והבנת מנגנון הפעולה של האינטרפרונים אלפא וביתא, עשויים לסייע בשיפור טיפולים רפואיים המבוססים על אינטרפרון (האינטרפרונים, הממלאים תפקיד חשוב ב"כיוונון" המערכת החיסונית והפעלתה, משמשים לטיפול בחולי סרטן ומחלות נגיפיות שונות).
פורצים את המנעול
ד"ר שרייבר וחברי קבוצת המחקר שלו הניחו ששורש התעלומה מונח במבנה התצמיד שכל אחד מהאינטרפרונים יוצר עם אחד משני הקולטנים המתאימים להם, המוצגים על פני התאים. כדי לבחון את ההשערה הזאת הם השתמשו בטכניקות של הנדסה גנטית ויצרו גרסאות (מוטציות) שונות של אחד מהקולטנים לאינטרפרון. לאחר מכן בחנו את אופן הפעולה של מגוון הקולטנים המוטנטים, וגילו שאחת מהגרסאות יצרה קשר מסוים עם אינטפרון אלפא, וקשר שונה עם אינטרפרון ביתא.
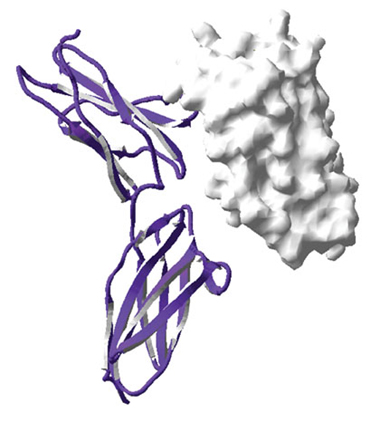
בשלב זה החלו המדענים להתמקד בגילוי האופי המבני, התלת-ממדי, המדויק של התצמיד בין אותו קולטן לאינטרפרון לבין אינטרפרון אלפא. בתחילה ניסו לבחון את התצמיד בטכנולוגיה הקרויה קריסטלוגרפיה בקרני X ("רנטגן"). כדי להפעיל את השיטה הזאת יש ליצורמהתצמיד הנבחר גבישים, שאותם מפציצים בקרינת X חזקה. בחינת ההתפזרות של הקרינה שפוגעת בגביש עשויה לרמוז על המבנה המרחבי של התצמידים אשר כלולים בו. המדענים ניסו אפוא ליצור גבישים מהתצמיד שבין האינטרפרון לקולטן שלו, אך לרוע המזל הדבר לא עלה בידם. לנוכח מצב העניינים הזה, החליטו ד"ר שרייבר וחברי קבוצת המחקר שלו לבחור בטכניקה אחרת, הקרויה "עגינה" ("דוקינג"), המבוססת על שימוש במודלים ממוחשבים.
דרושים שניים לטנגו
אלא שכאן נתקלו בקושי נוסף: כדי להפעיל את שיטת העגינה ביעילות, יש צורך במידע על המבנה של שני ה"שותפים". דרושים שניים לטנגו. אבל לרוע המזל, בשלב זה לא היה בידיהם מידע על המבנה של הקולטן. לפיכך החליטו להשתמש במודל תיאורטי של החלבון הזה. אלא שכאן נתקלו בקושי נוסף: בטכנולוגיות הקיימות קשה מאוד להשתמש במודלים תיאורטיים לצורך הפעלת שיטת העגינה. לפיכך החליט צוות המחקר לפתח שיטת עגינה ייחודית, שמשתמשת בנקודות מגע בין שני החלבונים. באמצעות הטכנולוגיה החדשה החלו המדענים לחפש את נקודות העגינה שבין האינטרפרון לבין הקולטן התיאורטי. גילוי נקודות העגינה האלה מספק רמזים טובים על מבנה התצמיד, ועל מבנה הקולטן. דרך פעולה זו, של הפעלת שיטת ה"עגינה" על מודל תיאורטי של חלבון (ולא על מבנה ידוע), נוסתה לראשונה על ידי ד"ר שרייבר וחברי קבוצת המחקר שלו. הצלחת השיטה נחשבת לפריצת דרך בחקר המבנה המרחבי של חלבונים.
נקודות העגינה הן הנקודות שבהן חומצות אמיניות שמרכיבות את האינטרפרון נוגעות בחומצות אמיניות "תיאורטיות" הכלולות במודל של הקולטן (מולקולות חלבון, דוגמת אינטרפרון והקולטן שלו, מורכבות מרצף שלמולקולות קטנות יותר, של חומצות אמיניות). למטרה זו השתמשו בשיטה הקרויה "מעגל מוטנטי כפול", שפיתח פרופ' אמנון הורוביץ, ראש המחלקה לביולוגיה מבנית במכון ויצמן למדע. שיטה זו מבוססת על הכנסת מוטציות לרצפים של החלבונים הנבחנים, ובחינה ממוקדת של השפעת הגומלין בין הגרסאות התיאורטיות השונות של מולקולת הקולטן לבין המוטציות שבוצעו בפועל במולקולת האינטרפרון. ואכן, לאחר בדיקה של יותר ממאה שילובים שונים בין זוגות של חלבונים (גרסאות מוטנטיות של אינטרפרון ומודלים תיאורטיים שונים של הקולטן שלו), הצליחו ד"ר שרייבר ותלמידי המחקר לילה רויזמן ויעקב פילר לזהות חמישה זוגות של חומצות אמינו המשמשות "נקודות מגע" בין החלבונים.
בשלב זה התקשרו המדענים להרולד שראגה, ביוכימאי מאוניברסיטת קורנל בארה"ב, שתיכנן אלגוריתם יעיל להפקת מידע על המבנה של חלבונים על-פי מיפוי נקודות העגינה שלהם בתצמיד שהם יוצרים עם חלבונים אחרים. הרצת נתוניהם של המדענים הישראליים באמצעות האלגוריתם של שראגה הניבה רמזים משמעותיים ראשונים על מבנהו של התצמיד החמקמק. מבנה זה מספק הסבר טוב למגוון הרחב של תוצאות שהתקבלו בניסויים קודמים, והוא גם פותח פתח ליצירת אינטרפרון שיהיה פעיל יותר מהאינטרפרון הרגיל.
כיצד, אם כך, האינטרפרונים אלפא וביתא, המתקשרים לקולטנים זהים, מפעילים גנים שונים? ד"ר שרייבר: "מבנה התצמיד שפיענחנו מצביע על כך שהפעלת הגנים השונים לא נובעת מהבדלים באופן שבו שני סוגי החלבונים (אינטרפרון אלפא וביתא), נקשרים לקולטן זה". לכן מתמקדים עכשיו החוקרים בפיענוח הקישור של האינטרפרון לקולטן נוסף, וכן לקישור של אינטרפרונים לשני קולטנים בעת ובעונה אחת.