01-01-1999
בקרה גנטית של התגובה החיסונית
מדעני המכון גילו - עוד בשנות השישים - את הקשר בין הרקע הגנטי לבין התגובות החיסוניות המתחוללות בגוף. השיטה התגלתה באמצעות ניצול של אנטיגנים סינתטיים פשוטים יחסית, להשגת שליטה ובקרה על תגובות חיסוניות בזנים של עכברים מוכלאים. האנטיגנים הסינתטיים, המשמשים מעין דגם של חלבונים, שהרכבם נקבע בצופן הגנטי, שימשו במקרה זה להדגמת ולבחינת השינויים שמתחוללים בתגובות החיסוניות, כתוצאה משינויים גנטיים מסוימים.
של מי מוח העצם הזה
מדעני המכון פיתחו שיטה המאפשרת להשתיל בגופם של חולי לוקמיה תאי מוח עצם שמקורם בתורם לא-תואם. השתלות מסוג זה נחשבו במשך זמן רב "לא אפשריות", בשל הדחייה שמפעילה המערכת החיסונית של החולה, נגד תאים זרים. הוויתור על התאמה קרובה מאוד בין התורם למקבל עשוי להרחיב במידה ניכרת את האפשרות להשתיל מוח-עצם בחולי לוקמיה.
לוקמיה היא מחלה דמויית סרטן, הניכרת ביחסים כמותיים לא תקינים בין תאי הדם השונים. מכיוון שכל תאי הדם נוצרים מ"תאי גזע" המצויים במוח העצם, מניחים החוקרים שהמחלה נובעת מתפקוד לא תקין של "תאי הגזע". כדי לתקן את הליקוי הזה הורסים הרופאים (באמצעות הקרנות וחומרים כימותרפיים) את מוח העצם בגופם של החולים. לאחר מכן שותלים - במקום הרקמה ההרוסה - תאי מוח עצם, שבהם גם "תאי גזע" תקינים. הבעיה היא שבשלב זה נכנסת לפעולה המערכת החיסונית של החולה, הדוחה את התאים הזרים. מדעני המכון מציעים להתגבר על התופעה הזאת באמצעות השתלת "מנות-ענק" של מוח-עצם, המתגברות על דחיית המערכת החיסונית.
כאן נכנס לתמונה קושי נוסף: כמות מוח העצם שאפשר לקחת מתורם היא מוגבלת למדי. לפיכך, החליטו החוקרים להגדיל את כמות תאי הגזע הנשתלים באמצעות איסופם של תאים אלה ממחזור הדם ההיקפי. כדי לישם את השיטה הזאת מגדילים החוקרים (באמצעות תכשירים הורמונליים) את כמות תאי הגזע שבדם, ולאחר מכן מפרידים את "תאי הגזע" המיועדים להשתלה.
טעות חוזרת
מחלות אוטו-אימוניות הן מחלות שבהן המערכת החיסונית של הגוף, שנועדה להגן עליו מפני פולשים ומזהמים זרים, טועה בזיהוי ותוקפת את הרקמות הבריאות של הגוף, או חומרים החיוניים לפעולתו התקינה. בין המחלות האלה אפשר למנות טרשת עורקים, טרשת נפוצה, סוכרת נעורים, דלקת פרקים שגרונית, זאבת אדמנתית ועוד. מדעני המכון פיתחו שיטה לגידול התאים ה"טועים" של המערכת החיסונית בתרביות רקמה, ולשימוש בהם כבתכשירים העשויים לשמש מעין תרכיבי חיסון נגד המחלות הללו. הגישה החדשה מצויה בעיצומה של בדיקה קלינית, המתבצעת במקומות שונים בעולם.
רותמים את המוות למען החיים 1
חוקרי המכון גילו שתאי המערכת החיסונית (תאי דם לבנים מסוג T), ההורגים תאים נגועים, מבצעים את משימתם כשהם מפעילים בתאי המטרה (הנקטלים) מעין "תוכנת התאבדות" ייחודית, הגורמת להם לאבד את עצמם לדעת. מדובר ב"תוכנה" גנטית פנימית הטמונה בכל תאי הגוף (לרבות תאי ה- T עצמם), המורה להם לאבד את עצמם לדעת - ובמותם לצוות לגוף את החיים. תופעה זו של השמדה עצמית קרויה אפופטוסיס (ביוונית "השלה", או "השרה", כינוי שנובע מהדמיון שבין התופעה לבין תהליך השלכת שבו מתים עלי העצים בסתיו).
חוקרים אחרים במכון גילו את מרכיבי השרשרת הביוכימית שבאמצעותה התאים מאבדים את עצמם לדעת. מתברר שהשרשרת הזאת קצרה בהרבה מכפי שסברו במשך שנים רבות. היא מתחילה בקולטן שמוצג על קרומו של התא וקולט מסרים כימיים שונים הבאים מסביבתו החיצונית של התא. אזור מסוים של הקולטן השקוע בתוך תא המטרה נצמד ומפעיל חלבון שכונה בקיצור "מוות 1", וזה נצמד ומפעיל אנזים מסוים (MACH), המתפקד כ"כלי נשק" שבאמצעותו התא מאבד את עצמו לדעת. האנזים מבקע חלבונים מסוימים החיוניים לתא, ובכך הוא גורם למות התא. חוקרי המכון גילו ושיבטו את הגנים האחראיים לייצורם של החלבון "מוות 1" ושל האנזים MACH.
ההבנה שהושגה במחקרים אלה, באשר לתהליכי המוות של תאים, עשויה לאפשר תכנון וביצוע מניפולציות שונות שיחזקו או יחלישו את יכולתה של המערכת החיסונית להילחם בתאים ש"נכבשו" על-ידי גורמים זרים (חיידקים או נגיפים), בתאים סרטניים, או בתאים שרק "נראים" לה, בטעות, כ"אויבים" (טעות שעלולה לגרום להתפרצות של מחלה אוטו-אימונית, דוגמת טרשת נפוצה, דלקת פרקים שגרונית, סוכרת נעורים, ועוד).
על הפרק
מדעני המכון גילו שנוגדנים ממשפחת הגאמא-גלובולין מאיצים את גידולם של גבישי מלח נתרני של חומצת השתן (נתרן אוראטי) במפרקי הגוף של חולים במחלת הצינית (גאוט). החוקרים מיצו את נוגדני הגאמא-גלובולין מנוזלי הפרקים של חולי צינית, ובשורת ניסויים הראו - במבחנה - כי הנוגדנים האלה יכולים להאיץ את היווצרות ושקיעת הגבישים. ייתכן שתהליך זה הוא אחד מהגורמים להתפתחות המחלה.
לכאורה נראה שהנוגדנים פועלים במקרה זה בדרך שונה מהדרך שבה פועלים רוב סוגי הנוגדנים: כשהם נקשרים לגורם מסוים, הם לא נאבקים בו והורסים אותו, אלא להיפך, הם "משתפים פעולה" עמו, ומסייעים לו לגדול ולהתפתח. בעקבות זאת הציעו החוקרים תפיסה חדשה שלפיה אתר הקישור של הנוגדנים "זוכר" את מבנה הגביש של נתרן אוראטי, דבר שמאפשר לנוגדנים להכיר ולייצב גבישונים חדשים של המלח ולהאיץ את גידולם.
מחקר זה עשוי לסייע בהעמקת ההבנה של הדרך שבה נוגדנים מזהים גופים זרים, וכן בהבנת מנגנון הפעולה של מחלת הצינית ומחלות אחרות שקשורות בהיווצרות גבישים בגוף.
מושכים אש
מיאסטניה גראוויס היא מחלה המתבטאת בחולשת שרירים קשה, הנובעת מהפרעה במעבר אותות מהעצב לשריר. מדעני המכון מצאו שהחולים במחלה זו מייצרים בגופם נוגדנים שתוקפים חלבון מוגדר בצומתי התקשורת שבין השרירים לעצבים. בהמשך זוהו שברים פפטידיים של החלבון הזה, המהווים מטרות להתקפותיה של המערכת החיסונית. ממצא זה הוביל לתכנון "חיקויים" סינתטיים של הפפטידים האלה, המיועדים "למשוך אליהם את האש" של המערכת החיסונית, ולהסיטה מהחומרים הטבעיים החיוניים לפעילותו התקינה של הגוף. פיתוח זה עשוי להוות ציון דרך חשוב במלחמה במחלת המיאסטניה גראוויס.
יוצרים נוגדנים
חוקרי המכון נמנו עם חלוצי הייצור של נוגדנים חד-שבטיים (כלומר, נוגדנים זהים לחלוטין זה לזה, שמקורם בתאים זהים) בתרביות רקמה, בחיידקים ובבעלי חיים; והיו הראשונים שהפעילו את הטכנולוגיה הזאת בישראל. נוגדנים חד-שבטיים שהוכנו במכון שימשו למחקר בסיסי, וכן לפיתוח מבדקי איבחון הקשורים, בין השאר, בהריון ובמחלות ממאירות. תכשירים אחרים שמדעני המכון פיתחו על בסיס נוגדנים חד-שבטיים מסייעים לקידום המחקר בתחום ההבנה והבלימה של תהליכי אלרגיה, לפיתוח גישות חדישות למניעת התפתחותם של גידולים סרטניים, ולפיתוח מודלים לניסויים בתחום חקר המחלות האוטו-אימוניות (מחלות המתחוללות כשהמערכת החיסונית תוקפת - בטעות - רקמות בריאות של הגוף וחומרים החיוניים לפעולתו התקינה).
נוגדנים מתקשרים
מדעני המכון זיהו את אתר הקישור של הנוגדנים, את מיקומו ואת מבנהו. אתר זה ממוקם בקצה השרשרת החלבונית המשתנה ב"זרועותיו" של הנוגדן (נוגדנים הם מבנים המורכבים מכמה שרשרות פפטידיות היוצרות את צורת האות האנגלית Y). החוקרים מיפו את האזור באתר הקישור הבא במגע עם האנטיגן (שאליו נצמד הנוגדן), ובנו מודל מרחבי שלו. מודל זה סייע רבות בהבנת תהליכי ההתקשרות של נוגדנים לאנטיגנים. בנוסף לכך גילו מדעני המכון כי בנוגדן מתחולל שינוי מבני לאחר התקשרותו לאנטיגן.
נוגדן מלאכותי
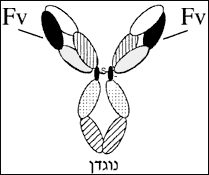
מדעני המכון פיתחו את הנוגדן הסינתטי הראשון בעולם (בדרך הטבע, נוגדנים מיוצרים בגוף בתאי דם לבנים מסוג B). לאחר מכן הכינו המדענים, לראשונה, את המקטע הקטן ביותר של נוגדן הכולל את כל תכונות הקישור של הנוגדן. מקטע זה (הקרוי Fv), משמש כיום, בשיטות של הנדסה גנטית, ליצירת "ספריות" של נוגדנים סינתטיים לריפוי מחלות שונות. גודלו של המקטע הזה הוא כשישית מגודלו של נוגדן שלם, דבר שמקל על חדירתו לרקמות.
תאים מחוץ לגוף
מדעני המכון היו הראשונים שפיתחו שיטה לשיבוט וליצירת תרביות תאי T פעילים של המערכת החיסונית (לימפוציטים), מחוץ לגוף. שיטות אלה מופעלות כיום בידי חוקרים רבים במקומות שונים בעולם, בתחום חקר המחלות האוטו-אימוניות (מחלות שמתחוללות כאשר המערכת החיסונית תוקפת - בטעות - רקמות בריאות של הגוף או חומרים החיוניים לפעולתו התקינה).
נוגדנים וכימותראפיה
מדעני המכון פיתחו נוגדנים הנצמדים באופן בררני למרכיבים מסוימים המופיעים על קרומיהם של תאים סרטניים. נוגדנים אלה יכולים לשמש לזיהויים ולסימונם של התאים הסרטניים. הם גם יכולים לפעול כ"טילים מונחים", ולהוביל אל התאים הממאירים תרופות שישמידו אותם.
במחקר אחד, למשל, שילבו החוקרים את הנוגדנים האנטי-סרטניים עם תאי T של המערכת החיסונית. תאים אלה נועדו לזהות, להשמיד ולדחות תאים זרים (כגון שתל של רקמות מתורם זר), תאים של הגוף שנגיפים או חיידקים "השתלטו" עליהם, וכן גם תאים סרטניים הנודדים בדרכם להקמת גרורות סרטניות חדשות. אלא שבנסיבות מסוימות, תאי T לא מצליחים למלא את ייעודם ואינם מזהים תאים סרטניים. במקרים אלה מצליחים התאים הסרטניים לחמוק וליצור גרורות סרטניות.
מדעני המכון צירפו, בטכניקות של הנדסה גנטית, את הספציפיות של נוגדנים חד-שבטיים אנטי-סרטניים עם תאי T . השילוב החדש הוכיח את יעילותו בניסויים במעבדה, ונבחן עתה בשלבים מוקדמים של ניסויים קליניים.
האינטרפרונים באים
מדעני המכון גילו את הגן האחראי לייצורו של קולטן לאינטרפרון אלפא, חומר המשמש מעין שליח של המערכת החיסונית, הגורם להפעלתה של המערכת החיסונית כנגד פולשים זרים שונים, ובעיקר כנגד נגיפים. סימנים שונים מראים כי רמות חריגות של אינטרפרון-אלפא בדם מחמירות מחלות אוטו-אימוניות מסוימות (מחלות הנגרמות כאשר המערכת החיסונית תוקפת - בטעות - רקמות בריאות של הגוף, או חומרים שונים החיוניים לפעילותו התקינה), ולפיכך נראה שקולטני האינטרפרון שבודדו ושובטו על-ידי חוקרי המכון פותחים אפשרויות לתכנון תרופות חדשות נגד המחלות האלה.
במחקר אחר פיתחו מדעני המכון דרך לייצור תעשייתי של אינטרפרון ביתא, בשורות (תרביות) תאים של בעלי חיים. עד אז אפשר היה לייצר כמויות תעשייתיות של אינטרפרון ביתא רק בחיידקים שהמטען הגנטי שלהם שונה לשם כך. אינטרפרון ביתא משמש לטיפול במחלות שונות, ובהן גם טרשת נפוצה. האינטרפרון ביתא שמיוצר בשיטה שפיתחו מדעני המכון, גורם פחות השפעות לוואי בהשוואה לאלה שנגרמות כתוצאה משימוש באינטרפרון ביתא שמיוצר בחיידקים (וזאת, מכיוון שהוא דומה יותר לאינטרפרון ביתא שמיוצר באופן טבעי בגוף האדם).
מכוונים את המערכת החיסונית
מדעני המכון גילו ובידדו חלבון שעשוי לשמש בסיס לבלימת מחלות אוטו-אימוניות. בסוגים אחדים של מחלות מסוג זה מעורב החלבון אינטרלוקין - 6, המשמש מעין "שליח כימי" שמעורר את המערכת החיסונית לתגובה התקפית, והחיוני לחיותם של התאים יוצרי הנוגדנים. החלבון שבידדו מדעני המכון (הקרוי רסטריקטין - P), מתקשר לתאי המערכת החיסונית ו"משדר" אליהם "מסר" שמבטל את "מסר החיים" של האינטרלוקין - 6. בכך, למעשה, הוא עלול לגרום למותם (ולבלום את התרבותם) של חלק מהתאים יוצרי הנוגדנים, דבר שמחליש פעילויות מסוימות של המערכת החיסונית. יכולת ממוקדת ובררנית זו, להחליש חלקים של התגובה החיסונית, עשויה לשמש לפיתוח שיטות טיפול ומניעה של מחלות אוטו-אימוניות.

