עיתונאיות ועיתונאים, הירשמו כאן להודעות לעיתונות שלנו
הירשמו לניוזלטר החודשי שלנו:
התאים המרכיבים גידולים סרטניים במוח הם מגוונים ביותר ויוצרים לעיתים מבנים תלת-ממדיים ייחודיים. כבר בשנת 1932 ניסה הנוירוכירורג האמריקאי פרסיבל ביילי לתת בהם סימנים וגילה כי ניתן לזהות בגידולים אלה כמה משפחות של תאים המציגים תכונות דומות. תשעה עשורים אחרי, עדיין ידוע מעט מדי על זהותן של קבוצות התאים המרכיבות גידולי מוח מסוגים שונים, על המבנים המסודרים שהן יוצרות ועל האופן שבו הן משפיעות על מהלך המחלה ואפשרויות הטיפול בה. בהתאם, שיעורי ההצלחה של הטיפולים במרבית סוגי סרטן אלו אינם גבוהים לרוב.
בעשור החולף, הבשילה טכנולוגיית הריצוף של חומר גנטי ברמת התא הבודד והיא מאפשרת כיום לחוקרים לנתח בפירוט, בבת אחת, אלפי תאים החיים באותה סביבה בגוף, להבין אילו גנים הם מבטאים, לסווגם לקבוצות וללמוד על התפקיד של כל קבוצה. במעבדתו של ד"ר איתי תירוש במחלקה לביולוגיה מולקולרית של התא במכון, בשיתוף פעולה עם קבוצתו של פרופ' מריו סובה מבית-החולים הכללי של מסצ'וסטס (MGH), רתמו טכנולוגיה זו על מנת לצלול מחדש לשאלות הפתוחות בתחום סרטן המוח.

הסוג השכיח ביותר של גידולי מוח הוא גליומה – גידולים שמקורם בתאי תמך המסייעים לתאי העצב. גידולי גליומה נחלקים לשניים – גידולים עם מוטציה בגן המקודד לאנזים בשם IDH שדרגת החומרה שלהם נמוכה לרוב, וגידולים אלימים במיוחד שאין בתאיהם את אותה מוטציה מסוימת ושמם בשפה הרפואית גליובלסטומה. במחקרים מהשנים האחרונות, פענחה קבוצתו של ד"ר תירוש באמצעות שיטות של ריצוף החומר הגנטי ברמת התא הבודד, את ההרכב התאי של גידולים משני הסוגים. הם גילו כי תאי הגידולים נחלקים לקבוצות שכל אחת מהן מבטאת תוכנית גנים ייחודית, הקובעת באיזה "מצב" ביולוגי יהיו תאי הסרטן בקבוצה. בין היתר, זיהו החוקרים קבוצות תאים שמחקות באמצעות תוכניות הגנים הייחודיות תאים תקינים במוח.
כעת, במחקר שהתפרסם לאחרונה בכתב-העת המדעי Cell, רתמו מדענים ממעבדתו של ד"ר תירוש, בהובלת ד"ר אליסה גרינוולד, נעם גלילי וד"ר רובן הופלין, טכנולוגיות המאפשרות לא רק לרצף את החומר הגנטי ברמת התא הבודד אלא גם למפות את ביטויו במרחב. שיטות אלו אפשרו לחוקרים לזהות לראשונה אילו גנים מתבטאים באופן ייחודי בכל אחת מאלפי נקודות שונות במבנים המרחביים של הגידולים המוחיים. כך יכלו המדענים למפות במדויק כיצד מתארגנים במרחב גידולי גליובלסטומה וגליומה. לשם כך הם בחנו דגימות מגידולים של 13 חולי גליובלסטומה ו-6 חולי גליומה עם מוטציה ב-IDH.
הממצאים מעידים כי הכוח שמניע את הגידול להסתדר במבנה שכבתי הוא המחסור בחמצן המתעצם עם התקדמות המחלה והתפתחות הגידול
התגלית הראשונה של החוקרים הייתה שקבוצות התאים השונות בתוך גידולי גליומה אינן מפוזרות באופן שווה בכל רחבי הגידול, אלא מרוכזות בסביבות שונות בתוך הגידול. אותן מיקרו-סביבות אינן הומוגניות לגמרי, שכן בקרבת תאים מסוג מסוים ניתן היה למצוא תמיד גם בני קבוצות אחרות. בשלב הבא, בדקו החוקרים אם ישנן קבוצות תאים בגידול שחיות בדרך כלל בשכנות זו לזו וגילו כי לא רק שישנם שכנים מועדפים, אלא שזיווגים אלה של שכנות טובה הינם עקביים בחולים שונים.
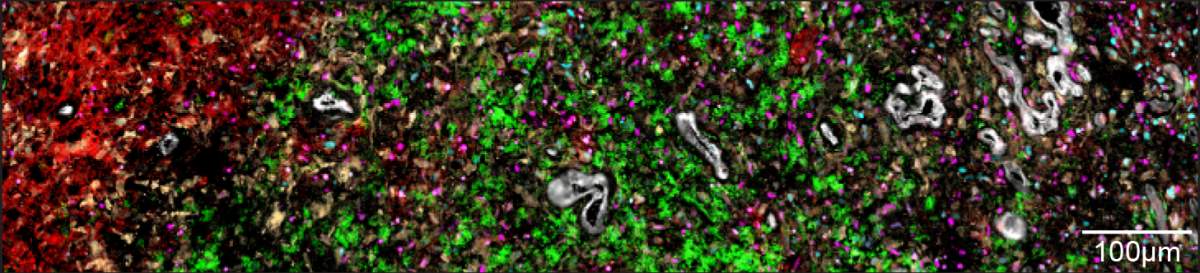
זוגות מסוימים של שכנים חיקו את ההתנהגות הטבעית של רקמות במוח: כך למשל, תאים שמחקים תאי אב של תאי תמך מסוג אוליגודנדרוציטים נמצאו בקרבת תאי אנדותל, תאים המרכיבים את דופן כלי הדם. זיווג זה מתקיים גם ברקמה הבריאה, שכן תאי אנדותל מפרישים חומרים הנדרשים להישרדות ולהתרבות של תאים קדם-אוליגודנדרוציטים. בדומה, תאים שמחקים תאי אב של תאי עצב שכנו בגידול באזורים שבהם הוא חודר לתוך רקמת המוח הבריאה, כשם שתאי אב ברקמה בריאה נודדים עם התחדשותה. ועדיין, מרבית הזיווגים שהתגלו אינם מובנים במלואם.
במבט-על, זיהו החוקרים כי התארגנותן של קבוצות התאים בסביבות נפרדות בגידול יצרה חמש שכבות נבדלות. השכבה הפנימית או ליבת הגידול, היא רקמת נמק שבה תאים שאינם מקבלים מספיק חמצן כדי להתקיים. בשכבה שסביב לנמק נמצאו תאים דמויי רקמת חיבור עוברית ותאים נוספים ובהם תאים של המערכת החיסונית האחראים למצבי דלקת. בשכבה השלישית ניתן היה למצוא בעיקר כלי דם, תאי אנדותל המרכיבים את דופן כלי הדם, וכן תאים נוספים של המערכת החיסונית.
בשתי השכבות החיצוניות יותר של הגידול, התאים כבר אינם סובלים ממחסור בחמצן. עובדה זו מאפשרת את התפתחותן של קבוצות תאי גידול המחקות רקמות מוח נורמליות בשכבה הרביעית – תאי אב של תאי עצב ותאי תמך. השכבה החיצונית ביותר כוללת את רקמת המוח הבריאה שלתוכה חודר הגידול. הממצאים על השכבות השונות של הגידול מעידים כי הכוח שמניע את הגידול להסתדר במבנה שכבתי הוא המחסור בחמצן המתעצם עם התקדמות המחלה והתפתחות הגידול.
בהתאם לממצאיהם, הבחינו המדענים כי גידולים בדרגה קלה יותר - שהם בדרך כלל גם קטנים יותר - וכן אזורים בגידול עם אספקת חמצן טובה הציגו מבנה כאוטי. כך למשל בגידולי גליומה עם IDH מוטנטי, לא הייתה לרוב רקמת נמק והם הציגו מבנה בלתי מסודר; במקרים החריגים שבהם הייתה רקמת נמק, הדגימות ניחנו גם במבנה מסודר למדי.
"חשפנו כי המבנה המרחבי המסודר מאפיין גידולים אגרסיביים בדרגת חומרה גבוהה יותר", מתאר ד"ר תירוש. "רמת החמצן בסביבת המחיה של תאי הגידול משפיעה על תוכנית הגנים שהם מבטאים ובכך על המצב שלהם. בהתארגנות זו של הגידול, נוצרות שכבות מובחנות שיכולות להיות נגישות פחות לתרופות ולתאי המערכת החיסונית, וכך הן עשויות להפוך את הגידול לעמיד יותר".
במעבדתו של ד"ר תירוש השתמשו בידע שצברו על הרכב התאים בגידולי גליומה על מנת להבין כיצד תרופה חדשה ומבטיחה מסייעת לחלק מהחולים בסרטן זה. לשם כך השתמשו המדענים בדגימות מגידולי סרטן של שלושה חולים שהשתתפו בניסוי הקליני בתרופה והגיבו לטיפול, וכן שש דגימות מחולים שלא טופלו כלל. להשלמת התמונה, הם הסתמכו גם על נתוני דגימות מ-23 חולים שטופלו בתרופה ו-134 חולים שלא טופלו בה.
המדענים, בהובלתו של ד"ר אבישי שפיצר, זיהו שהתרופה אשר פועלת באמצעות מנגנון המעכב את ייצורו של האנזים IDH בגרסתו הסרטנית, גורמת לתאים לשנות את תוכנית הגנים שהם מבטאים. למעשה, הטיפול מעודד את תאי הגזע הסרטניים להתמיין לתאים בוגרים, וכך נפגעת יכולתם להתחלק במהירות – והתקדמות המחלה נבלמת.

המדענים שיערו כי אם התרופה פועלת באמצעות התמיינות של תאי גזע סרטניים לתאים בוגרים, מוטציה הפוגעת בגן החיוני לתהליך ההתמיינות עשויה להסביר את המקרים שבהם התרופה אינה עובדת. בדגימות מחולים שלא טופלו בתרופה, הם זיהו מוטציה בגן מסוים שקשורה לשיעור נמוך של תאי סרטן בוגרים ושיעור גבוה של תאי גזע סרטניים. כאשר השתיקו את אותו גן במודל סרטן בעכברים, הם ראו כי התרופה אכן לא הובילה לאפקט הטיפולי המיוחל. "ממצא זה מראה שמוטציה בגן שזיהינו יכולה להוות סמן ביולוגי שיאפשר להבחין מראש בין חולים שיפיקו תועלת מהטיפול וכאלו שלא", מסביר ד"ר תירוש. הממצאים החדשים עשויים לסייע גם במציאת טיפול המשלב בין מעכבי IDH לתרופה נוספת שתעודד את תהליך ההתמיינות ותגביר את השפעת הטיפול על הגידול הסרטני.
"שני המחקרים האחרונים שלנו חושפים את הכוחות שמעצבים את אופיים של תאי הסרטן בגידולי מוח, בין אם זו סביבת המחייה שלהם בתוך הגידול או התערבות תרופתית המשנה את תוכנית ביטוי הגנים בתאים", מסכם ד"ר תירוש. "ממצאים אלה פותחים צוהר לגישה חדשה לטיפול בסרטן, שכן אם אנחנו מכירים את קבוצות התאים המאכלסות כל אזור בגידול הסרטני ויודעים כיצד תא יכול לעבור ממצב אחד למשנהו, ייתכן שנוכל לפתח טיפולים ממוקדים חדשים שישנו את מהלך המחלה. ההבנה שהרכב התאים בתוך הגידול והמבנה התלת-ממדי שלו קשורים למידת האגרסיביות, יכולה גם להוליד שיטות אבחון חדשות שאינן מסתמכות רק על נפח הגידול והמוטציות שלו".
במחקר על מבנה גידולי גליומה השתתפו גם ד"ר דור סימקין, יותם הרניק וד"ר ג'ולי לאפי מהמחלקה לביולוגיה מולקולרית של התא במכון; ד"ר כריסטופר מאונט, ד"ר ניקולס גונזלס קסטרו, סידני דומונט, ד"ר מסשי נמורה וד"ר ואמסי מנג'ינה מבית החולים הכללי של מסצ'וסטס (MGH) ובית הספר לרפואה של הרווארד בבוסטון, ארה"ב; דנה הירש מהמחלקה למשאבים וטרינריים במכון; תום טלפיר מהמחלקה למדעי המחשב ומתמטיקה שימושית במכון; ד"ר מירב קדמי, ד"ר אינה גוליאנד, ד"ר הדס קרן-שאול וד"ר יוסף אדדי מהמחלקה לתשתיות מחקר מדעי החיים במכון; ג'ואל מדיצ'י, פרופ' מייקל ולר וד"ר מריאן כ. ניידרט מבית החולים האוניברסיטאי של ציריך, שוויץ; וד"ר באוגו לי מהמחלקה לאימונולוגיה מערכתית במכון.
במחקר על הטיפול במעכבי IDH מוטנטי השתתפו גם ד"ר רוני חנוך-מאיירס מהמחלקה לביולוגיה מולקולרית של התא במכון; ד"ר סיימון גריטש, ד"ר מסשי נמורה, האנה וייסמן, ד"ר ניקולס גונזלס קסטרו, ניקולס דראק, ג'ון לי, רווינדרה מילווגנם, רייצ'ל לי סרוויס, ג'רמי מאן פאנג, פרופ' כריסטין ק. לי, ד"ר הירואקי נגשימה, פרופ' ג'ולי מילר, ד"ר איזבל ארילאגה-רומני, ד"ר דיוויד לואיס ופרופ' הירואקי וואקימוטו מבית החולים הכללי של מסצ'וסטס (MGH) ובית הספר לרפואה של הרווארד בבוסטון, ארה"ב; ד"ר ג'רום פורטין ממרכז הסרטן על שם הנסיכה מרגרט בטורונטו ומאוניברסיטת מקגיל במונטריאול, קנדה; ד"ר ראמיה רבירם, פרופ' דן לנדאו וד"ר דניאל קייהיל ממרכז הגנום של ניו יורק, ארה"ב; ויל פיסאנו ופרופ' קית' ליגון מבית החולים בריגהאם אנד וימנ'ס בבוסטון, ארה"ב; פרופ' פטריק וון ממכון דנה-פרבר לסרטן של אוניברסיטת הרווארד בבוסטון, ארה"ב; פרופ' טק מאק מאוניברסיטת הונג קונג; פרופ' מארק סנסון וד"ר מהדי טואט מאוניברסיטת סורבון בפריז, צרפת.
משך ההישרדות החציוני של המאובחנים בגליובלסטומה הוא 14 חודשים בלבד ושל המאובחנים באוליגודנדרוגליומה דרגה 2 (סוג של סרטן גליומה עם IDH מוטנטי) הוא 11 שנים.