עיתונאיות ועיתונאים, הירשמו כאן להודעות לעיתונות שלנו
הירשמו לניוזלטר החודשי שלנו:
טיפול כימותרפי בסרטן יכול להציל חיים, אך הוא כרוך בסיבוכים חמורים, כולל זיהומים. עד עכשיו, הקריטריון העיקרי להערכת סיכון זה היה מספר תאי הדם: אם מספרם של תאי דם לבנים נמוך מערך סף קריטי, הסיכון נחשב גבוה. מודל חדש שפיתחו מתמטיקאים ממכון ויצמן למדע, בשיתוף עם רופאים מהמרכז הרפואי מאיר בכפר סבא וממרכז המחקר הופמן לה-רוש בבזל, שווייץ, מראה, כי לצורך הערכת הסיכון חיוני לקבוע לא רק את כמותם של תאי הדם אלא גם את איכותם, אשר משתנה מאדם לאדם.
המחקר מהווה צעד חשוב בהתפתחות התחום הצעיר של רפואה מותאמת אישית: הוא עשוי להוביל לגישה אישית יותר לכימותרפיה. לדוגמה, בחולים בסיכון גבוה, יצטרכו הרופאים לנקוט באמצעים מוגברים כדי למנוע זיהום. מחולים בסיכון נמוך, לעומת זאת, אפשר יהיה לחסוך טיפולי מנע מיותרים.
המחקר התפרסם באחרונה בכתב-העת המדעי Journal of Clinical Investigation, ובוצע על-ידי קבוצת חוקרים מתחומים שונים למדי: מתמטיקה שימושית, הנדסת חשמל, אונקולוגיה, אימונולוגיה ורפואת ילדים.
 המודל החדש מסביר כיצד פועלת מערכת החיסון בתנאי נוטרופניה, כלומר רמה נמוכה של תאי דם לבנים, בעיקר מסוג נויטרופילים. במצב זה, הנוצר לעיתים קרובות לאחר כימותרפיה או השתלת לשד עצם, אך עשוי להיות גם מולד, עלולים להתפתח זיהומים חמורים במידה ומערכת החיסון אינה מצליחה לבצע את תפקידה החיוני: בליעה וחיסול של חיידקים. "המודל המתמטי שלנו גילה מנגנונים חדשים האחראים להבדלים במידת הפגיעות לזיהומים בין חולי נוטרופניה", אומרת ראש הקבוצה, פרופ' ורד רום-קדר, מהמחלקה למדעי המחשב ומתמטיקה שימושית במכון ויצמן למדע.
המודל החדש מסביר כיצד פועלת מערכת החיסון בתנאי נוטרופניה, כלומר רמה נמוכה של תאי דם לבנים, בעיקר מסוג נויטרופילים. במצב זה, הנוצר לעיתים קרובות לאחר כימותרפיה או השתלת לשד עצם, אך עשוי להיות גם מולד, עלולים להתפתח זיהומים חמורים במידה ומערכת החיסון אינה מצליחה לבצע את תפקידה החיוני: בליעה וחיסול של חיידקים. "המודל המתמטי שלנו גילה מנגנונים חדשים האחראים להבדלים במידת הפגיעות לזיהומים בין חולי נוטרופניה", אומרת ראש הקבוצה, פרופ' ורד רום-קדר, מהמחלקה למדעי המחשב ומתמטיקה שימושית במכון ויצמן למדע.
המודל מראה, כי במצב של נוטרופניה אי אפשר להסביר את יחסי הכוחות בין תאי החיסון לבין החיידקים באמצעות היחס הפשוט בין מספר התאים למספר החיידקים, או באמצעות קביעת ערך סף מינימלי לכמות תאי החיסון. הסיבה לכך היא, שכשספירת הנויטרופילים נמוכה, נכנסת מערכת החיסון של החולה למצב של איזון עדין – הקרוי, במונחים מתמטיים, "דו-יציבות". מצב זה עשוי להיות מופר באופן דרמטי על-ידי שינויים זעירים בריכוז החיידקים או במספר הנויטרופילים. גורמים נוספים אשר עשויים להשפיע באופן דרמטי על איזון זה כוללים את מידת היעילות של הנויטרופילים, או מידת חדירות הרקמות לחיידקים – זו עלולה לגדול בגלל טיפולים כימוטרפיים.
כך, על-פי המודל, באנשים בריאים אין חשיבות רבה לכך שתפקוד הנויטרופילים משתנה מאדם לאדם. בחולים עם נוטרופניה, לעומת זאת, עשויים הבדלים אלה להוות הבדל בין חיים למוות. מסקנה זו מבוססת על מחקר אשר התבסס על בדיקות שנערכו בדמם של ארבע מתנדבים בריאים. כדי ליישם את המודל בפרקטיקה יש לערוך ניסוי קליני מקיף.
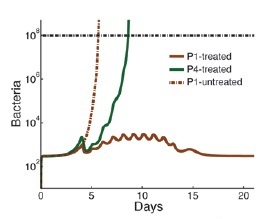
המודל כבר הציע פתרונות למספר תעלומות רפואיות. הוא מסייע להסביר, למשל, מדוע חולי סרטן מסוימים מפתחים זיהומים מסכני חיים אחרי כימותרפיה, למרות שהם מוחזקים בבידוד בתנאים סטריליים. מתברר שאם הנויטרופילים שלהם "חלשים", די בכמות זעירה של חיידקים, כגון זאת הקיימת דרך קבע במעיים, כדי להטות את האיזון העדין לטובת החיידקים.
המחקר מסביר גם מדוע חולים מסוימים מפתחים זיהום חמור לאחר כימותרפיה או השתלת לשד עצם, אפילו כאשר מספר הנויטרופילים שלהם חוזר לרמה נורמלית יחסית. כאמור, הכימותרפיה גורמת לא רק להפחתה במספר הנויטרופילים ולהחלשת התפקוד שלהם, אלא גם מגבירה את חדירותן של רקמות החולים לחיידקים. המודל מראה כי כתוצאה מכך, בחולים מסוימים, ריכוז החיידקים עולה במהירות גבוהה כל כך, עד כי אפילו חזרת הנויטרופילים לערכים הנורמליים לא מצליחה להתגבר על החיידקים – אשר הספיקו בינתיים להתרבות בפראות. תסריט זה עשוי להסביר בעתיד גם את המקרים הנדירים בהם מתפתחים זיהומים חמורים בבני אדם בעלי מערכת חיסון רגילה. על-פי המודל, במקרים אלה התרבות מהירה של חיידקים אלימים במיוחד עלולה לגבור על פעילותם של הנויטרופילים, אפילו אם מספרם ויעילותם תקינים.
המודל גם עשוי לסייע לרופאים לפענח מקרים רפואיים חסרי הסבר. לדוגמה, תינוק שטופל במרכז הרפואי מאיר בעקבות נוטרופניה מולדת הבריא, למרות שספירת הנויטרופילים שלו הייתה נמוכה מ-200 תאים למיקרוליטר דם. לעומת זאת, חולה סרטן בוגר נפטר כאשר ספירת הנויטרופילים שלו לאחר כימותרפיה עמדה על 380. המודל מסביר כיצד פרמטרים קליניים, כגון איכות ירודה של הנויטרופילים, יכלו להוביל דווקא למות החולה הבוגר למרות העדיפות המספרית של הנויטרופילים שלו.
בנוסף, המודל עשוי לסייע בהבנת התפתחותם של זיהומים חמורים חוזרים בחולים מסוימים. רופאים מהמרכז הרפואי מאיר הצליחו לקבוע אבחון רק בשליש מבין כאלף חולים שהופנו אליהם עקב זיהומים חמורים. המודל המתמטי של מדעני מכון ויצמן מציע כי לפחות חלק מהמקרים הלא פתורים נבע כנראה מצירוף של מספר פגמים אימוניים, כמו הבדלים בתפקוד הנויטרופילים ותאים אימוניים אחרים.
את המחקר ביצעו חוקרים המשלבים תחומי התמחות באופן בלתי שגרתי. ראש הקבוצה, המתמטיקאית פרופ' ורד רום-קדר, מתמחה בחקר מערכות דינמיות. המחבר הראשון, ד"ר רועי מלכה, הוא מהנדס חשמל שביצע את המחקר במסגרת לימודי הדוקטורט שלו במכון ויצמן, וכיום מבצע מחקר בתחום דומה בבית הספר לרפואה של אוניברסיטת הרווארד. את הרעיון למחקר הגה ד"ר אליעזר שוחט, אונקולוג בכיר, גם הוא בעל תואר דוקטור במתמטיקה ממכון ויצמן. כעת הוא עובד במרכז מחקר של חברת התרופות הופמן לה-רוש בבזל שבשווייץ. במחקר השתתפה קבוצה מהמרכז הרפואי מאיר: פרופ' ברוך וולך, ראש המעבדה לתפקוד לויקוציטים וראש הקתדרה לאימונולוגית ילדים בפקולטה לרפואה על שם סאקלר באוניברסיטת תל אביב, ומנהלת המעבדה רונית גבריאלי, שביצעה את הניסויים.
פרופ' וולך: "מהמחקר עולה כי כדי להגיע לתוצאות אופטימליות בכימותרפיה או בטיפול בחולים עם זיהומים חוזרים, רצוי לבדוק גם את איכות הנויטרופילים של החולים ואת ריכוז החיידקים בהם. בדיקות כאלה תסייענה בהפחתת תחלואה ומוות, וכמו כן בהפחתת הוצאות אישפוז ומתן תרופות יקרות. יתירה מזאת, ייתכן כי בדרך זו יתאפשר צמצום השימוש באנטיביוטיקה, ובכך יתאפשר להפחית את התפתחותם של זני חיידקים העמידים לתרופות".
מידע נוסף אפשר לקבל במשרד דובר מכון ויצמן למדע: 08-934-3856