הגנום של הסרטן הוא מכלול הדי-אן-אי של התא הממאיר. כל סוג של סרטן מתאפיין בפגמים מסוימים בגנום. קבוצתו של ד"ר גץ במכון ברוד, הכוללת כ-30 ביולוגים, ביוכימאים, פיסיקאים ומהנדסי תוכנה, לוקחת חלק בפרויקט "האטלס של גנום הסרטן", שמנהלים מכוני הבריאות הלאומיים של ארה"ב, ובפרויקטים נוספים המכוונים לאותה מטרה: פענוח הגנומים של כל סוגי הסרטן העיקריים.
פרויקטים שאפתניים אלה התאפשרו בזכות הטכנולוגיה החדשנית שפותחה לפני כמה שנים, high-throughput sequencing, המאפשרת "לקרוא" מקטעי די-אן-אי רבים במקביל. היא הובילה להאצה דרמטית של ריצוף הדי-אן-אי, וגם לירידה לא פחות דרמטית בעלותו: מ-30 אלף דולר בשנת 1999 למיליון "אותיות" די-אן-אי, ל-10 סנט בשנת 2011. כתוצאה מכך יכולים המדענים כעת לרצף במהירות מאות גנומים של גידולים סרטניים, כל אחד מהם כולל מיליארדי זוגות של בסיסי די-אן-אי. אך בריצוף די-אן-אי אין די: לא פחות מאתגר להבין מה טמון במבול הזה של מידע גנומי.
קבוצתו של ד"ר גץ במכון ברוד מפתחת כלים חישוביים לניתוח מידע זה. בביקורו במכון ויצמן, בדצמבר 2008, שאל גץ את דומאני, המנחה שלו לשעבר, האם מישהו מתלמידיו הנוכחיים יהיה מעוניין לקחת חלק במחקר זה. דומאני המליץ על יותם דרייאר. העובדה שגץ ודרייאר באים מרקע דומה – שניהם שירתו בצה"ל במסגרת "תלפיות", שבמהלכה שניהם קיבלו תארים אוניברסיטאיים במתמטיקה ובמדעים מדויקים אחרים (גץ בפיסיקה, דרייאר במדעי המחשב) – הבטיחה שיתוף פעולה פורה.
כך אכן קרה. דרייאר פיתח אלגוריתם הקרוי BreakPointer, אשר סורק את כל הגנום האנושי ומוצא את סימני ההיכר של הסרטן: פגמים בתיקון הדי-אן-אי המובילים לחילופים מבניים שהם שונים מרצף הדי-אן-אי הרגיל. היה זה האלגוריתם הראשון שהצליח לזהות את נקודות השבירה המדויקות בדי-אן-אי בהן מתרחשים החילופים. "הכלי הזה הוא חלק חשוב ובלתי-נפרד כעת מהמאמץ שלנו למפות את כל הגנים ואת כל התופעות התורמות לסרטן", אומר ד"ר גץ.
ה-BreakPointer השתלב בכל הניתוחים של גנום הסרטן במכון ברוד, וכבר סייע במספר תגליות מדעיות משמעותיות, כולל גילוי השיבושים שעל שמם הוא קרוי: נקודות השבירה המובילות לחילופים בדי-אן-אי.
כפי שדווח בכתב-העת
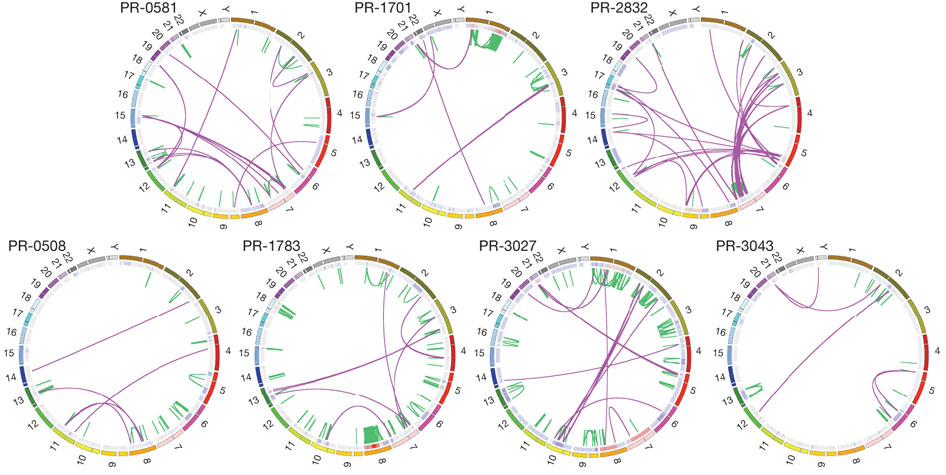
Nature, ה-BreakPointer עזר לגלות דפוס חילופים בכרומוזומים בסרטן הערמונית שלא היה ידוע עד אז: שרשראות מורכבות של חילופים בתוך גנים של סרטן או לידם. יתר על כן, המדענים גילו קשר בין מיקום נקודות השבירה לבין מצב הכרומטין, מרכיב חשוב באריזת המגן של הכרומוזומים, דבר המצביע על כך שחילופים גנומיים עשויים להיות קשורים לא רק לגנים,
אלא גם לגורמים אפיגנטיים, כלומר, כאלה שאינם מקודדים ישירות בגנום.
במחקר על סרטן של המעי הגס, שהתפרסם בכתב-העת
Nature Genetics, גילו המדענים באמצעות האלגוריתם 11 חילופי די-אן-אי שהובילו לגנים מאוחים בצורה לא נורמלית. ביניהם היה גן "סדרתי", המופיע במספר רב של גידולים שונים – וגן ראשון מסוג זה התגלה בסרטן המעי הגס. גנים המחוברים בצורה לא נורמלית מייצרים חלבונים לא נורמליים, ואלה יכולים להוות בעתיד מטרה לטיפולים ממוקדים, לא רק מפני שהם חיוניים לקיומו של הסרטן, אלא גם כי הם אינם קיימים בתאים בריאים, ולכן הטיפול יוכל להתמקד בתאי הגידול מבלי לפגוע ברקמות בריאות.
"ה-BreakPointer מזהה את המיקום המדויק של השבירות בדי-אן-אי באמצעות איתור רצפים 'חשודים' בגנום הסרטני, והשוואתם לאזורים המתאימים בגנום נורמלי", אומר ד"ר דרייאר, כיום חוקר בתר-דוקטוריאלי בבית ספר לרפואה של הרווארד ובמכון ברוד. "בעזרת האלגוריתם מצאנו קשרים אפשריים בין חילופים בדי-אן-אי לבין איפיונים אחרים של הגנום, כגון מוטציות או מצב הכרומטין". קשרים אלה ומשמעותם הביולוגית בסוגי סרטן שונים תוארו באחרונה בכתב-העת המדעי Genome Research.
המיפוי של כל גנומי הסרטן העיקריים יאפשר למדענים להבין טוב יותר את התהליכים המולקולריים הגורמים לסרטן, ובכך יקדם את פיתוח התרופות המותאמות לפגמים הגנומיים הייחודיים של כל גידול. טיפולים ממוקדים מסוג זה כבר קיימים לגבי כמה סוגי סרטן, ומספרם גדל כל הזמן. בעתיד ימפו הרופאים באופן שוטף את הגנום של כל החולים בסרטן, במטרה להתאים לכל אחד טיפול אישי, יעיל ובטוח.