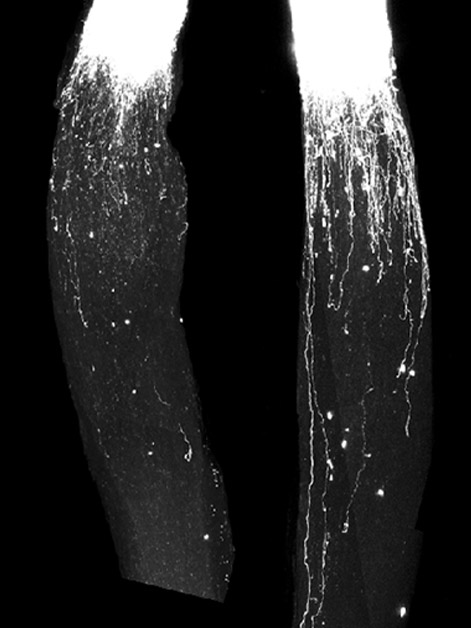
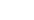בשונה מהמוח ומחוט השדרה, לתאי העצב ההיקפיים, אשר שלוחותיהם הארוכות מגיעות לעור ולאיברי הגוף, יש יכולת להתחדש לאחר פגיעה. זו הסיבה שפציעות במערכת העצבים המרכזית הן חשוכות מרפא, בעוד מפציעות בעצבים היקפיים ניתן להשתקם, גם אם לאורך חודשים או שנים. גם לאחר שנים רבות של מחקר, מנגנון התחדשות תאי העצב ההיקפיים לא פוענח במלואו. במחקר חדש ממעבדתו של פרופ׳ מיכאל (מייק) פיינזילבר במכון ויצמן למדע, שממצאיו מתפרסמים בכתב-העת המדעי Cell, נחשפה משפחה של מאות מולקולות אר-אן-אי שתפקידן לא היה ידוע עד כה, אך הן התגלו כחיוניות להתחדשות עצבית. באופן מפתיע, הראה צוות המחקר כי מולקולות אלה יכולות לעודד צמיחה בעכברים לא רק במערכת העצבים ההיקפית, אלא גם בזו המרכזית. הממצאים עשויים לסלול דרך לטיפולים חדשים בפגיעות עצביות מסוגים שונים ובמחלות ניוון מוחי.

התחדשות תא עצב היקפי מחייבת קודם כל ערוץ תקשורת בין גוף התא ובין השלוחה הארוכה שלו – האקסון – שיכולה להגיע לאורך של מטר ויותר בבני-אדם. בסדרת מחקרים לאורך 20 שנה, חשפה מעבדתו של פרופ׳ פיינזילבר מנגנון מרכזי בתקשורת הזו – חלבונים המשמשים כקרונות דואר ומשנעים מגוף התא אל האקסון הוראות לייצור חלבונים השולטים בגדילה התאית וחלבונים אחרים. התנועה של קרונות אלה בין גוף התא לאקסון ובחזרה, משמשת לא רק לשינוע הוראות הייצור אלא גם לאומדן המרחק בין גוף התא לקצהו, וכך היא מאפשרת לתא לווסת את מידת הצמיחה שלו. אך שאלה מרכזית נותרה פתוחה: מה מעורר את פרץ הגדילה וההתחדשות לאחר פגיעה מלכתחילה, ומדוע צמיחה זו אינה מתרחשת בתאים של מערכת העצבים המרכזית?
""ההאצה בגדילה שהראינו במחקר היא עדיין לא כזו שתיתן פתרון למצבי שיתוק קליניים, אך היא בהחלט ניכרת"
במחקר החדש, בחן ד"ר אינדרק קופל ממעבדתו של פרופ' פיינזילבר, בשיתוף ד"ר ריקי קוואגוצ'י מ-UCLA, אילו גנים מתבטאים לאחר פציעה בתאי עצב היקפיים בעכברים ועשויים אולי להסביר את פרץ הצמיחה. הוא הופתע לגלות כי יממה לאחר פגיעה עצבית, הגבירו התאים את הביטוי של משפחה שלמה של מקטעים גנטיים קצרים בשם B2-SINEs, שתפקידם לא היה ידוע עד כה. מקטעים אלה אינם מקודדים לחלבון כלשהו ומשום שהם נוהגים לקפוץ ממקום למקום בגנום, וישנו סיכון שיופיעו במקום הלא נכון בזמן הלא נכון, יצא להם שם רע. המדענים זיהו כי לאחר פציעה, תא העצב ההיקפי מתחיל לייצר תעתיקים רבים – מולקולות אר-אן-אי – של אותם מקטעים גנטיים מסתוריים, במקביל לתהליכים אחרים של הכנה לצמיחה ותיקון התא.
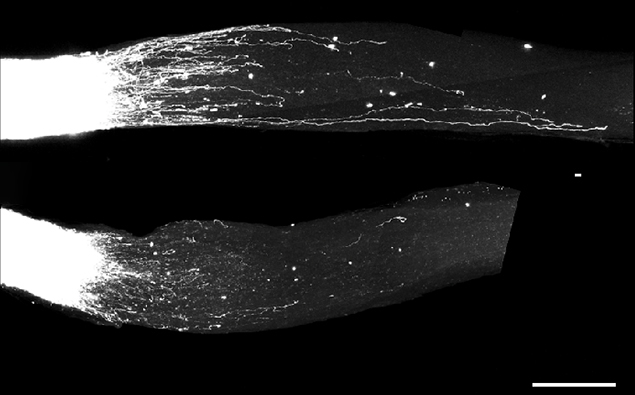
אבל B2-SINE היא משפחה ענקית של 150 אלף מקטעים גנטיים הפזורים ברחבי הגנום העכברי, והבדיקה הראשונית שבוצעה לא הסגירה מי מהם אחראי לגדילה. ד"ר איתן ארז זהבי ממעבדתו של פרופ׳ פיינזילבר, שהוביל את המחקר החדש לצד ד״ר קופל, השתמש בכלים ביואינפורמטיים כדי לזהות 453 מתוכם המתבטאים ביתר שאת לאחר פציעה ומעודדים גדילה. בשיתוף קבוצות מחקר מרחבי העולם, הראו המדענים כי ייצור היתר של אותן מולקולות לאחר פציעה ייחודי לתאים ההיקפיים, וכי הוא אינו מתרחש במערכת העצבים המרכזית.
המרכז בעקבות הפריפריה
המדענים החליטו לבדוק האם יוכלו להשתמש במולקולות שנמצאו בתאים ההיקפיים כדי לעודד צמיחה גם בתאי עצב של מערכת העצבים המרכזית. הם גרמו לתאי עצב מסוימים ברשתית העין של עכבר לייצר כמויות גדולות של אר-אן-אי מסוג B2-SINE וראו כי חלה האצה בהתחדשות שלהם לאחר פציעה. בנוסף, נבדק תרחיש של פגיעה עצבית בתאי קליפת המוח המוטורית – אזור במוח ששולט בתנועת השרירים באמצעות אקסונים ארוכים הנשלחים לחוט השדרה. המדענים הראו כי תאי קליפת המוח המוטורית בעכברים שביטאו רמות גבוהות של B2-SINEs התחדשו מהר יותר לאחר שנגדעו האקסונים שלהם בחוט השדרה. "אין עדיין טיפולים יעילים להאצת צמיחה והתחדשות של תאי עצב", מדגיש פרופ׳ פיינזילבר. "אמנם ההאצה בגדילה שהראינו במחקר היא עדיין לא כזו שתיתן פתרון למצבי שיתוק קליניים, אך היא בהחלט ניכרת. כמובן שהדרך מהמחקר הבסיסי לקליניקה ארוכה וצריך לוודא למשל שהאצת מנגנוני הגדילה אינה מגבירה יתר על המידה את הסיכון לסרטן".

התעלומה האחרונה שנדרשו המדענים לפענח היא המנגנון שבאמצעותו מעודדות מולקולות האר-אן-אי התחדשות עצבית. בעזרת קבוצת המחקר של פרופ׳ אלמה ברלינגיים מ-UCSF הם הראו כי המולקולות מעודדות חיבור פיזי בין קרונות הדואר המובילים הוראות ייצור לחלבונים החיוניים לגדילה ובין הריבוזומים שקוראים את המתכונים ומייצרים אותם. מנגנון זה גורם לכך שפריקת קרונות הדואר וייצור החלבונים החיוניים לגדילה מתרחשים בשלב מוקדם מהרגיל, סמוך לגוף תא העצב ולא בקצה האקסון. המדענים משערים שכך למד התא שהוא קטן בהרבה מממדיו הרצויים ומאיץ את הצמיחה העצבית.
"ישנם יותר ממיליון מקטעים גנטיים באדם הנקראים אלמנטי Alu והם מקבילים ל-B2-SINEs בעכברים. אפילו הראו בעבר שמולקולות אלה נקשרות לריבוזומים ולקרונות הדואר, אך לא הבינו למה. אנו בודקים כעת האם אלמנטי Alu או מקטעי אר-אן-אי לא מקודדים אחרים מעורבים בהתחדשות עצבית בבני-אדם", אומר פרופ׳ פיינזילבר. "החלמה מפציעה שמערבת תאי עצב היקפיים או ממחלה מערכתית שפוגעת בהם כמו סוכרת, יכולה להיות ארוכה מאוד. בדיוק משום כך אנו בוחנים בימים אלה בשיתוף 'בינה' – היחידה למחקר טרום-יישומי במכון ויצמן למדע – טיפול שמחקה את הפעולה של B2-SINEs ועשוי לזרז את ההחלמה; מדובר במולקולות קטנות שישמרו על קרונות הדואר קרוב לגוף תא העצב, יחברו אותם לריבוזומים ויאיצו את הצמיחה".
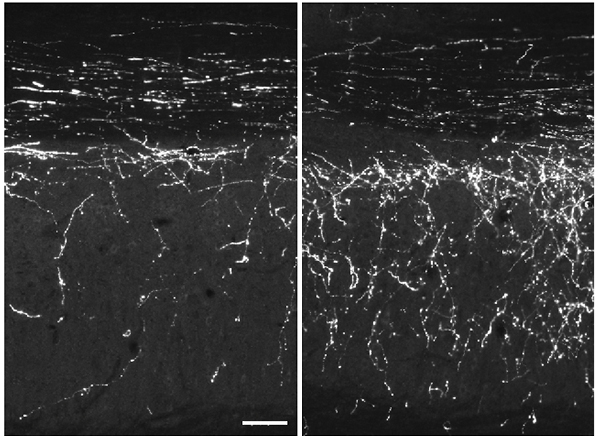
מעבר לעידוד הצמיחה בעצבים ההיקפיים, המחקר החדש חשף גם פוטנציאל מרחיק לכת עוד יותר: התחדשות במערכת העצבים המרכזית. "אנו בעיצומו של מחקר בשיתוף עם UCLA שמראה כי למנגנון שגילינו יש תפקיד בהחלמה משבץ מוחי במודל עכבר", מספר פרופ' פיינזילבר. "בנוסף, מחקר משותף של המכון, אוניברסיטת תל-אביב, האוניברסיטה העברית והמרכז הרפואי שיבא תל השומר, בודק את תפקיד המנגנון במחלת הניוון העצבי ALS. מחלות ניוון עצבי משבשות את חייהם של מיליונים, ואף שהדרך עוד ארוכה מאוד – כולי תקווה שבעתיד נוכל לרתום את מנגנון ההתחדשות שהתגלה לטיפול בהן״.