עיתונאיות ועיתונאים, הירשמו כאן להודעות לעיתונות שלנו
הירשמו לניוזלטר החודשי שלנו:
אילו מדענים היו יכולים להשתחל לצוללת מיקרוסקופית ולשייט בין תאי הגוף, כמו בסרט המסע הפנטסטי מ-1966, אחת התחנות הראשונות שלהם הייתה הכבד. מבנהו הייחודי של האיבר הפנימי הגדול בגופנו כולל יחידות פעולה קטנות דמויות משושה הנקראות "אוּניות" (lobules) ומבצעות כל אחת יותר מ-500 פעולות שונות במקביל. כבר בשנות ה-70 וה-80 התברר שתאי כבד מחלקים ביניהם את התפקידים הרבים בהתאם למיקומם בתוך כל תת-יחידה, אך הטכנולוגיה דאז אפשרה לקבל תמונה מעורפלת בלבד של חלוקה זו. במחקר חדש, המתפרסם היום בכתב-העת המדעי Nature, מציגים לראשונה מדעני מכון ויצמן למדע ועמיתיהם במרכז הרפואי שיבא ובמאיו קליניק אטלס גנטי של הכבד האנושי הבריא ברזולוציה של 2 מיקרון. הממצאים חושפים כי חלוקת התפקידים בכבד האנושי שונה מביונקים אחרים וענפה יותר ממה שהיה ידוע עד כה, ומראים כיצד היא הופכת אזורים מסוימים בכבד שלנו לפגיעים במיוחד לכבד שומני.

בשנים האחרונות הלכה והתפתחה טכנולוגיה שמאפשרת לזהות אילו גנים פעילים בכל תא ותא תוך מיקומם המרחבי המדויק של התאים על מפת הרקמה. עם זאת, למרות היכולות החדשות, מיפוי מדויק של חלוקת התפקידים בכבד האנושי התעכב, לא מעט בשל הקושי להשיג דגימות כבד מאנשים בריאים. בקבוצתו של פרופ' שלו איצקוביץ' במכון הבינו שהמפתח לפתרון הוא תרומות כבד אלטרואיסטיות; לכבד יכולת התחדשות מופלאה המאפשרת לאנשים לתרום חלק גדול ממנו לאדם הסובל ממחלה. כך בעזרת פרופ' עדו נחמני ופרופ' ניב פנקוביץ מהמערך לכירורגיה כללית במרכז הרפואי שיבא וד"ר טימוצ'ין טאנר ממרכז ההשתלות של מאיו קליניק במינסוטה, השיגו המדענים שמונה דגימות מתורמים בריאים והרכיבו אטלס של ביטוי גנטי בכבד האנושי.
"אלפי גנים התגלו כפעילים ברמות שונות בתאי כבד במקומות שונים, מה שמעיד על ארגון פנימי מדויק ומורכב בהרבה משחשבנו", אומר פרופ' איצקוביץ'. "במקום החלוקה הגסה לשלושה אזורי פעילות, שמקובלת כבר עשרות שנים, האטלס חשף שמונה אזורים בעלי תפקידים מובחנים. המיפוי המדויק של הכבד מאפשר כעת לכל מעבדה בעולם לצלול לעומק הכבד ולחקור מדוע אזורים שונים פגיעים למחלות שונות. מחלות מטבוליות, למשל, נוטות להתחיל במרכז האונית, בעוד שדלקות נגיפיות ואוטואימוניות מופיעות בעיקר בשוליה. כמו כן, לסרטן כבד ולגרורות מסרטנים אחרים יש את המקומות המועדפים עליהן. המפתח להבין מדוע זה כך מצוי במידע הגנטי המדויק שאספנו".
""חלוקת התפקידים היעילה היא ברכה וגם קללה – היא לא תוכננה לתזונה המודרנית שופעת השומנים והפחמימות, והיא עשויה להסביר מדוע אנו נוטים לצבור שומן עודף בכבד"
במטרה להשוותם לבני-אדם, מיפו במעבדתו של פרופ' איצקוביץ' גם את הכבד הבריא בעכבר וכן ביונקים גדולים יותר, חזיר ופר, שלהם קצב חילוף חומרים וגודל אוניות כבד הדומים לאדם. בכל היונקים דם זורם באונית מהשוליים למרכז ומספק בדרך חמצן ומזון לתאים. כתוצאה ממסלול זה, בשוליים שוררים תנאי שפע ובמרכז מחסור. בכל היונקים שנבדקו, למעט האדם, תנאי המחסור במרכז האונית גרמו לכך שהתאים שם יהיו יחסית פעילים פחות, בעוד באדם התגלה כי מתבצעות בליבת האונית פעולות רבות, ובהן ייצור שומנים מעודפי אנרגיה, הרכבת סוכר מחומרים שאינם פחמימות בזמני רעב, סינון רעלים וייצור נוזל המרה שמסייע בעיכול.
הבדל בולט נוסף שהתגלה במחקר בין הכבד האנושי לזה של יונקים אחרים נוגע לאגירת סוכר. הכבד מתפקד כ"מכל הדלק" של גופנו באמצעות ספיגה יעילה של הסוכרים שאנו מעכלים בארוחות ושחרורם באופן מבוקר בין הארוחות. במחקר התגלה שבאדם ספיגת הגלוקוז ייחודית למרכזי האוניות ולא לשוליהן, כמו בעכבר.
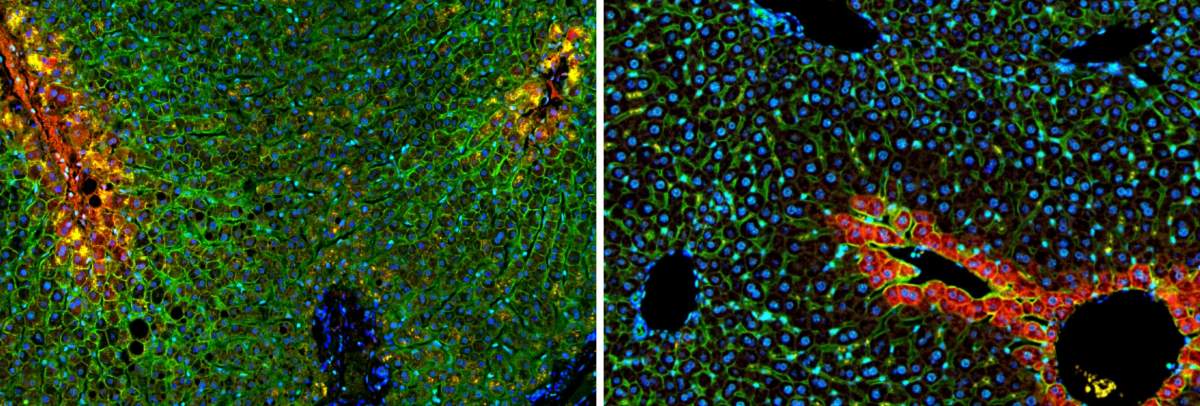
"חלוקת התפקידים הזו היא ברכה וגם קללה", מסביר פרופ' איצקוביץ'. "היא מאפשרת לכבד שלנו לאגור פחמימות ביעילות: תאים במרכז האונית קולטים ואוגרים סוכר (גלוקוז) ישירות מהדם, בעוד שתאים בשוליים ממירים לקטט לגלוקוז וכך תורמים גם הם למאגרי האנרגיה שמשמשים אותנו בצום. ואולם, חלוקת העבודה היעילה לא תוכננה לתזונה המודרנית ששופעת שומנים ופחמימות, ועשויה להסביר מדוע אנו נוטים לצבור שומן עודף בכבד ולסבול מהצטלקות שלו".
כדי להתמודד עם השחיקה ולמנוע מחלה, התפתח במרכזה של אונית הכבד האנושי מנגנון תחלופה ייחודי. "גילינו שבבני-אדם, בשונה מיונקים אחרים, סוג אחד של תאי חיסון מעדיף את ליבת האונית במקום לעמוד על המשמר בשוליה – שער כניסת הדם לרקמה", אומר ד"ר אורן יעקובובסקי ממעבדתו של פרופ' איצקוביץ', שהוביל את המחקר וגם מתמחה במערך לכירורגיה כללית במרכז הרפואי שיבא. "תאי 'קופפר' הם תאים בולעניים שמסוגלים להגן מזיהומים אך גם לבלוע, לפרק ולמחזר שאריות תאים שהתבלו. אנו משערים שהם 'עברו למרכז' באדם כדי להתמודד עם השחיקה המוגברת".
בחלקו האחרון של המחקר הראו המדענים כיצד האטלס החדש מסייע להתחקות אחר התפתחות מחלות. הם התמקדו במחלת הכבד השומני המטבולי, מצב נפוץ הקשור לעודף משקל וסוכרת, שבו שומן מצטבר בכבד ועלול להוביל לדלקת ולהצטלקות. ההשוואה בין תאים בריאים בכבד לתאים שהחלו לצבור שומן חשפה מנגנון הגנה: תאים שהחלו "להשמין" כיבו גנים שקשורים לייצור וקליטת שומן והפעילו גנים מסוימים שקשורים לפירוק. עם זאת, בכבד האנושי יש כשל שמגביל את יכולתו להתנגד להשמנה ביעילות: התברר שהצטברות שומן מובילה גם לירידה בייצור חלק מהרכיבים במיטוכונדריה – אברונים שמפרקים שומנים.
"על בסיס המיפוי המדויק של הכבד, ניתן יהיה בעתיד לפתח טיפולים שממוקדים בגנים שגורמים לאזור מסוים להיות פגיע במיוחד למחלה ספציפית", אומר פרופ’ איצקוביץ’. "יתרה מכך, המודל של בניית אטלס גנטי ברזולוציית תא בודד מדגימות של תורמים בריאים ניתן ליישום באיברים נוספים, שעד כה לא מופו במדויק באדם, וייתכן שהוא ישנה מהותית את האופן שבו אנו מבינים את מבנה ותפקוד הגוף האנושי".
במחקר השתתפו גם ד"ר קרן בהר הלפרן, ספיר שיר, רוי נובוסלסקי, ד"ר עדי אגוזי, ד"ר טל ברקאי, ד"ר יותם הרניק, ד"ר עמיחי אפריאט וד״ר יעל כורם כהנים מהמחלקה לביולוגיה מולקולרית של התא במכון; ד"ר חן מאיר וד"ר רון פרי מהמרכז הרפואי שיבא תל השומר; ד"ר רובן הופלין מאוניברסיטת פרייבורג, גרמניה; עפרה גולני, ד"ר אינה גוליאנד, ד"ר יוסף אדדי, ד"ר מירב קדמי וד"ר הדס קרן שאול מהמחלקה לתשתיות מחקר מדעי החיים במכון; ד"ר ליאת פלוס-אליגור, ילנה פריצ'יסלוב ודאנה הירש מהמחלקה למשאבים וטרינריים במכון.
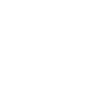
כרבע מהאוכלוסייה הבוגרת בעולם סובלת ממחלת הכבד השומני המטבולי והיא מחלת הכבד הנפוצה ביותר בעולם המערבי כיום.