קבוצת מדענים ממכון ויצמן למדע פיתחה שיטה המאפשרת להתגבר על מחלות אוטו-אימוניות באמצעות "הפניית האש" בחזרה אל גורמי המחלה. במחלות האלה, ובהן טרשת נפוצה, מחלת קרוהן ודלקת פרקים שגרונית, תוקפת מערכת החיסון בטעות את רקמות הגוף, וגורמת להן נזק. המדענים הצליחו לגייס לטובתם את מערכות החיסון של עכברים, ולגרום להן לתקוף את אחד השחקנים המחוללים את התהליכים האוטו-אימוניים – אנזים הקרוי MMP9. תוצאות המחקר התפרסמו באחרונה בכתב-העת
Nature Medicine.
משפחת האנזימים MMP, אליה שייך ה-MMP9, ממלאת תפקיד חיוני בתהליכים ביולוגיים שונים, בין השאר, ניידות והתרבות תאים וריפוי פצעים. אבל, כשחברים מסוימים מהמשפחה, ובעיקר MMP9, יוצאים משליטה, הם עלולים לסייע להתפרצות מחלות אוטו-אימוניות וליצירת גרורות סרטניות, על-ידי חיתוך לא מבוקר של ריקמות החיבור בגוף.
פרופ' אירית שגיא מהמחלקה לבקרה ביולוגית, וחברי קבוצת המחקר שלה, חיפשו בשנים האחרונות דרכים לחסום באופן ספציפי אנזימים השייכים למשפחה, דבר שעשוי להוביל לפיתוח טיפולים יעילים למספר מחלות.
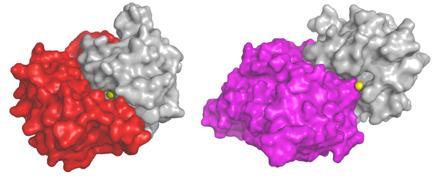
בעבר ניסו מדענים לחסום את חלבוני ה-MMP באמצעות תרופות המבוססות על מולקולות סינתטיות קטנות, שתוקפות ישירות את האנזימים. אך התברר להם, שהתרופות האלה אינן יעילות, ולעיתים אף גורמות תופעות לוואי קשות. כמו במקרים רבים אחרים, כחלק מתהליך הבקרה השוטפת של הגוף, הטבע כבר מצא פתרון אלגנטי לחסימת הפעילות של MMP בגוף. החסימה נעשית באמצעות חלבונים מעכבים, הקרויים TIMP, אשר פועלים בצורה מבנית מדויקת להפליא. חלבונים אלה כוללים זרוע הבנויה כך שתחדור במדויק לבקיע באנזים ה-MMP בו מצוי האתר הפעיל שלו (כלומר, האתר שבו מתבצעת התגובה הכימית אותה מבצע האנזים) – המורכב מאטום אבץ וסביבו שלוש חומצות אמינו מסוג היסטידין – ותסגור אותו כמו פקק מהודק. "לרוע המזל", אומרת פרופ' שגיא, "קשה מאוד לחקות את הדיוק הזה באמצעים מלאכותיים".
ד"ר נטע סלע-פסוול התחילה לעבוד על גישה חלופית לתרופות הקונבנציונליות כשהייתה תלמידת מחקר לתואר שני במעבדה של פרופ' שגיא, והמשיכה לחקור את התחום במסגרת מחקר הדוקטורט. ביחד עם פרופ' שגיא הוחלט, כי במקום לנסות לייצר מולקולה סינתטית שתתקוף ישירות את ה-MMP, הן ינסו למצוא "טריק" שיגרום למערכת החיסון ליצור נוגדנים כנגדם. הגישה שלהן הייתה, למעשה, יצירת מעין חיסון נגד צבר האבץ שבאתר הפעיל של ה-MMP9. בחיסונים נגד מחלות נגיפיות מחדירים לגוף חלקי נגיפים או נגיפים מומתים, הגורמים למערכת החיסון ליצור נוגדנים – שלאחר מכן יוכלו לתקוף גם נגיפים חיים. באופן דומה, כך שיערו המדענים, אפשר יהיה לחסן את הגוף נגד צבר האבץ שבאנזים ה-MMP, ולגרום למערכת החיסון ליצור נוגדנים מעכבי פעילות דומים למעכבים הטבעיים, ה-TIMP, אשר ייקשרו לאתר הפעיל של האנזים, ויחסמו אותו.
ביחד עם
פרופ' אברהם שנצר מהמחלקה לכימיה אורגנית במכון יצרו המדעניות את ה"חיסון": גרסה מלאכותית של צבר האבץ- היסטדין המצוי בלב האתר הפעיל של אנזים ה-MMP9. לאחר מכן הזריקו את גרסת החיקוי הסינתטית לעכברים, וחיפשו אם נוצרה פעילות חיסונית נגד MMP בדם העכברים. התברר, כי בדם העכברים אכן נמצאו נוגדנים חדשים. ניתוח מפורט של המבנה האטומי של הנוגדנים החדשים, שקיבלו את הכינוי metallobodies, גילה, כי שיטת פעולתם דומה לשיטה שמפעילים חלבוני ה-TIMP: הם שולחים זרוע לתוך הבקיע באנזים, וחוסמים את האתר הפעיל על-ידי קשירת צבר האבץ. נוגדנים אלה הראו בררנות: הם פגעו רק ב-MMP9 ובחבר משפחה נוסף (MMP2). כיוון שקיים דמיון רב בין ה-MMP9 העכברי לבין הגרסה האנושית, הנוגדנים יצרו קשרים חזקים גם עם הגרסה האנושית של האנזים.
כדי לבחון את הפעילות הביולוגית של הנוגדנים במחלה, גרמו המדענים לתסמונת דלקתית בעכברים המדמה את מחלת קרוהן. כפי שקיוו, הצליח הטיפול באמצעות נוגדנים למנוע את הופעת תסמיני המחלה.
"ההתרגשות נוכח שיטת החיסון החדשה קשורה לא רק לפוטנציאל שלה לטפל בעתיד במחלת קרוהן, אלא גם לאפשרות להשתמש בה כדי לנסות לפתח טיפולים חדשניים למחלות רבות נוספות שנגרמות על-ידי חלבונים המכילים צברי מתכת", אומרת פרופ' שגיא. חברת "ידע מחקר ופיתוח", המקדמת יישומים מסחריים על בסיס תגליות מדעני המכון, הגישה בקשה לרישום פטנט על מולקולות החיסון הסינתטיות, וכן על הנוגדנים הנוצרים בתגובה להן.
שותפים נוספים למחקר היו ד"ר אורלי דים, ד"ר חיים רוזנברג, ד"ר רענן מרגלית, ד"ר רינה ארד-ילין, וד"ר ציפי שוהם מהמחלקות לביולוגיה מבנית ולבקרה ביולוגית, רגאוונדה קיקארי מהמחלקה לכימיה אורגנית, ד"ר מירי אייזנשטיין מהמחלקה לתשתיות מחקר כימי, ד"ר אורי ברנר מהמחלקה למשאבים ווטרינריים, וד"ר תמר דנון מהמחלקה לביולוגיה מולקולרית של התא.