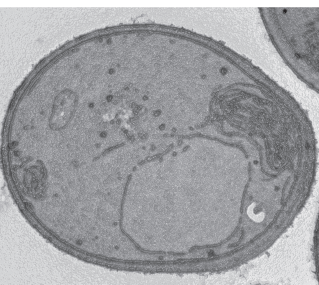
אגירת שומן בגוף אינה בהכרח רעיון רע; הכל תלוי היכן בדיוק השומן נאגר. מדעני מכון ויצמן למדע מצאו, כי מולקולות שומן הנאגרות בתוך "שקים" מיקרוסקופיים, שהם למעשה טיפות ליפידים (חומרים דמויי שומן), ממלאות תפקיד חיוני בחיי התא. הן משתתפות בהיווצרות מכונות מולקולריות אשר מבצעות את התהליך האוטופאגי, סוג של מחזור פירוק חומרים אשר שומר על מצבן התקין של רקמות הגוף, ומספק אנרגיה בעת הצורך. שיבושים בתהליך זה עלולים להוביל בין היתר לסרטן, למחלות נוירולוגיות או דלקתיות ועוד.
כאשר התהליך האוטופאגי עומד להתחיל, ה"ציוד" המולקולרי הדרוש לביצועו נבנה במקום: בתוך התא נוצר קרום שעוטף חלק מתוכן התא, והקרום הזה יוצר למעשה את האברון המאפשר מאוחר יותר את מחזור הפירוק התוך-תאי. עד עכשיו לא היה ידוע כיצד בדיוק נבנה הקרום הזה, וכיצד מתנהלת אספקת החומרים הדרושים לבנייתו.
פרופ' זבולון אלעזר, מהמחלקה לכימיה ביולוגית במכון ויצמן למדע, חוקר את התהליך האוטופאגי כבר יותר מעשור. יחד עם ד"ר תומר שפילקה (אז תלמיד מחקר), הוא גילה כי בתהליך זה מעורבות טיפות הליפידים. כפי שדווח באחרונה בכתבי-העת המדעיים
"רשומות האקדמיה הלאומית למדעים של ארה"ב" (
PNAS) ו-
EMBO Journal, המדענים גילו תחילה את הקשר בין התהליך האוטופאגי לבין יצירת מולקולות של חומצות שומניות. התברר, כי האנזים האחראי להפקת המולקולות האלה מפורק בתהליך האוטופאגי, אך כאשר הפירוק מסתיים – נעצר תהליך זה בתא. מכאן השתמע, כי יצירת החומצות השומניות היא תהליך אשר מבקר את עצמו. בנוסף, נראה היה כי תהליך זה חיוני לקיום התהליך האוטופאגי.
המדענים מצאו, כי לצורך האוטופאגיה דרושות מולקולות הקרויות פוספוליפידים, וכי מולקולות אלה חייבות להיווצר בזמן אמת מהחומצות השומניות ומחומרים האחרים אשר נאגרים בתוך טיפות הליפידים. בעבר נחשבו מולקולות השומן בתוך הטיפות בעיקר למאגרי אנרגיה, כמו רוב השומן בגופנו, אך המחקר החדש הראה כי הן מבצעות תפקידים הרבה יותר מתוחכמים וממוקדים, ומשמשות כאבני בניין עבור מכונות התהליך האוטופאגי.
בסדרת ניסויים, רובם מסתמכים על שינויים גנטיים, הראו המדענים כי טיפות הליפידים אכן חיוניות לאוטופאגיה: כאשר חסמו את היווצרות צבירי הליפידים, לא התקיים תהליך זה. יתר על כן, הטיפות נדרשו להימצא בזמן הנכון ובמקום הנכון כדי שהתהליך האוטופאגי יתקיים בהצלחה.
המדענים גילו גם, כי אברון גדול בשם רטיקולום אנדופלאסמי תורם ככל הנראה לבניית מכונות האוטופאגיה. הם מצאו, כי בין אברון זה לבין טיפות הליפידים התקיימו מגעים קרובים, אשר היו חשובים לבניית קרומי האוטופאגיה. המדענים זיהו מספר גנים האחראים להתפתחות מכונות האוטופאגיה וטיפות הליפידים.
מחקרים אלה בוצעו בשמרים, אך נראה כי התוצאות תקפות גם לתאי גוף האדם. יש לכך חשיבות, שכן האוטופאגיה מעורבת בתהליכים ביולוגיים רבים, וגם במחלות רבות. כך למשל, במצב רגיל ותקין מסייע התהליך האוטופאגי להגן על מערכת העיכול מפני חיידקים ופגמים בפעילותו הקשורים במחלות דלקתיות של המעיים, כגון מחלת קרוהן. בגידולים סרטניים, האוטופאגיה עוזרת לתאי סרטן לשרוד בתוך הגידול במצב של מחסור במזון ובחמצן. המדענים מקווים שבעתיד אפשר יהיה לפתח טיפולים למחלות אלה באמצעות שליטה על התהליך האוטופאגי.
צוות המחקר כלל את ד"ר אבלין ולטר, נועם בורובסקי, פרידה שימרון, ד"ר יואב פלג וד"ר נירה עמר, ונעשה בשיתוף עם מדענים מהולנד.