עיתונאיות ועיתונאים, הירשמו כאן להודעות לעיתונות שלנו
הירשמו לניוזלטר החודשי שלנו:
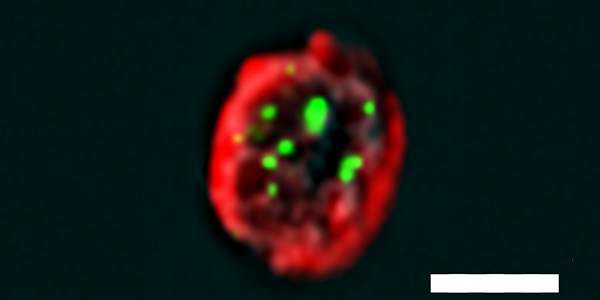
הטכנולוגיות הקיימות כיום מאפשרות לדעת כמעט הכל על הגנום האנושי מתוך דגימה של חומר גנטי מתא בודד. עם זאת, הצעד הנחוץ הבא – חקר החלבונים המקודדים על ידי הגנום – מחייב לעיתים קרובות לאסוף דגימות של מיליוני תאים, כמות שאינה זמינה כאשר מדובר בתאים נדירים המצויים בגוף בכמויות קטנות. במחקר שהתפרסם באחרונה בכתב-העת המדעי Nature Communications מציגים ד"ר יעקב אברמסון וקבוצתו, במחלקה לאימונולוגיה במכון ויצמן למדע, שיטה לחקר חלבונים בתא בודד שהופק מגוף חיה או אדם. לשם כך השתמשו המדענים בתאים נדירים הקרויים mTECs, המתַפקדים כמין "תצלומי סלפי" גנטיים, מפני שהם מציגים תמונה כמעט שלמה של הגנום: בשונה מתאים אחרים בגוף, ל-mTECs יכולת לבטא כמעט את כל הגנום המקודד חלבונים.
תאי ה-mTEC הם אמנם קמצוץ מתאי בלוטת התימוס (הֶרֶת), בלוטה המשמשת כמיפקדה ראשית של כוחות המערכת החיסונית, אך ללא תאים אלה, גופנו פשוט היה משמיד את עצמו. היות שתאים נדירים אלו מבטאים כמעט את כל הגנום המקודד חלבונים, הם מייצרים מעין "ספרייה" של כל חלבוני הגוף במטרה ללמד את המערכת החיסונית לא לתקוף חומרים אלה. לפיכך, תאי ה-mTEC יכולים גם להרוג או לנטרל תאי T אשר עלולים לפעול נגד רקמות הגוף עצמו, ובכך מונעים מקרים של "ירי מאש כוחותינו".
על מנת לחקור אינטראקציות בין חלבונים בתוך תא ה-mTEC, פיתחו תלמידת המחקר איילת אבין, החוקרת הבתר-דוקטוריאלית ד"ר מעיין לוי, וד"ר זיו פורת מהמחלקה לתשתיות מחקר מדעי החיים, שיטה חדשה הקרויה PLIC, שהיא שילוב של שתי טכנולוגיות: האחת מסמנת שינויים בחלבונים או אינטראקציות בין חלבונים באמצעות גלאים פלואורסצנטיים, והאחרת מזהה את המיקום של תגיות פלואורסצנטיות רבות בתא בודד. וכך, טכנולוגיה רגישה ביותר זו מאפשרת לאתר ולכמת שינויים בחלבונים או אינטראקציות בין חלבונים בתא בודד, גם כאשר החלבונים הללו נמצאים בכמויות מזעריות.

בעזרת שיטה זו הצליחו המדענים לגלות לפרטי פרטים – ולראשונה בסביבה הטבעית של תא המבודד מהגוף – את אחד המנגנונים שבאמצעותם מונע תא mTEC מהמערכת החיסונית לצאת למתקפה אוטואימונית. המדענים הראו, כי פעילות ה-mTEC נובעת מאינטראקציה בין שני חלבונים עיקריים: אחד המקודד על ידי גן הקרוי AIRE, ואחר המקודד על ידי גן בקרה הקרוי SIRT1. הם מצאו גם, כי SIRT1 מפעיל את AIRE כשהוא מסיר ממנו תג כימי של קבוצת אצטיל. בנוסף הראו המדענים, באמצעות השיטה, כי חלבוני AIRE נקשרים זה לזה ויוצרים קומפלקסים פעילים – בדיוק כפי שעלה ממחקריו הקודמים של ד"ר אברמסון.
לדברי ד"ר אברמסון, תובנות אלה עשויות לאפשר הבנה טובה יותר של מחלות אוטואימוניות, שכן הן יכולות לכוון מדענים אל הפגמים הגנטיים ואל המנגנוניים הגורמים מחלות אלה. כך למשל, העובדה ש-SIRT1 מעורב במניעת מתקפות אוטואימוניות מצביעה על כך, שמוטציות או "איות שונה" בגן זה עלולים לתרום להיווצרות מספר מחלות אוטואימוניות. המחקר עשוי גם לעזור להבין כיצד בדיוק עלולות מוטציות בגן AIRE לחולל מחלות אוטואימוניות. מסביר ד"ר אברמסון: "ישנם יתרונות רבים ליכולת לחקור אינטראקציות בין חלבונים ברמה של תא בודד. כך אפשר לחקור תאים נדירים כפי שהם בגוף, ללא עיוותים הנוצרים כאשר מְגַדלים תאים רבים מאוד מחוץ לגוף בצורה מלאכותית".
מדעני המכון הראו, כי ניתן להשתמש ב-PLIC לא רק ב-mTECs, אלא גם בתאים נוספים. לכן, פרט לתרומתה לחקר מחלות אוטואימוניות יכולה השיטה החדשה לתרום לחקר תאי גזע, תאים נדירים ברירית הפנימית של המעיים, או סוגים אחרים של תאים הנמצאים בגוף בכמויות קטנות ביותר.
על אף שתאי ה-mTEC מייצגים פחות מ-0.1% מתאי בלוטת התימוס, הם מבטאים את המספר הרב ביותר של גנים בגוף שלנו – יותר מ-90% מהגנום המקודד חלבונים. #מספרי_מדע |